С помощью CRISPR прямо сейчас происходит грандиозный прорыв в генной инженерии: ученые планируют скоро научиться избавлять нас навсегда от любых болезней, с перспективой любых контролируемых мутаций и вечной жизни.
На публикацию этого поста нас натолкнуло видео “CRISPR: редактирование генов изменит все и навсегда”, в котором рассказывается о переднем крае науки в части генной модификации человека: речь идет не просто об избавлении от болезней типа СПИД, рак и многие другие, но и о создании безупречного нового вида людей, людей со сверхспособностями и бессмертии. И это происходит прямо сейчас на наших глазах.
Все эти перспективы открываются благодаря недавнему революционному открытию белка CRISPR–Cas9, но обо всем по порядку.
Раньше считалось, что ДНК в каждой нашей клетке – абсолютно идентичны и содержат нашу точную и неизменную копию – какую клетку бы ни взять, но оказалось, что это не так: ДНК в разных клетках немного разные и они меняются в зависимости от разных обстоятельств.

Открытию белка CRISPR – Cas9 помогли наблюдения за выжившими после атаки вирусов бактериями.
Древнейшая война на земле
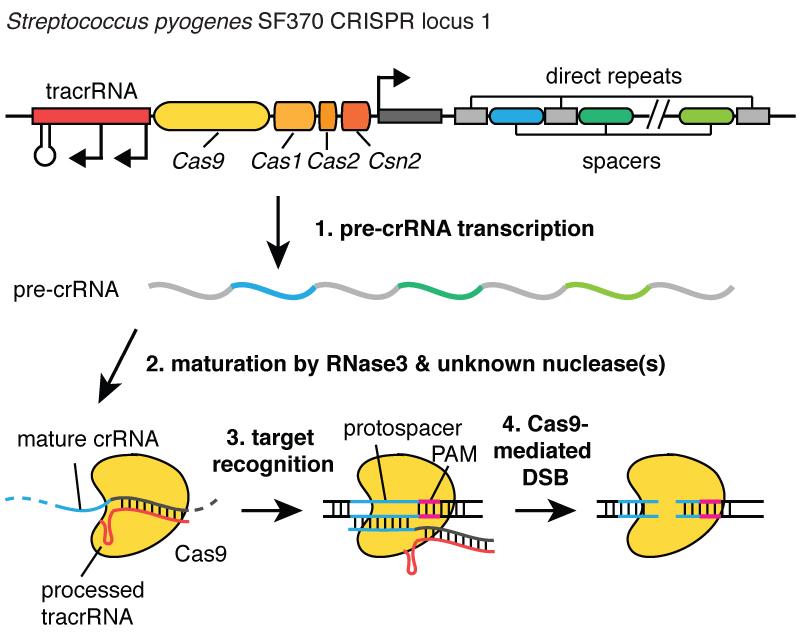
Бактерии и вирусы соперничают с начала жизни: вирусы-бактериофаги охотятся на бактерии. В океане они убивают 40% от общего числа бактерий каждый день. Вирус делает это, вставляя свой генетический код в бактерию и использует её в качестве фабрики.
Бактерии пытаются безуспешно сопротивляться, но в большинстве случаев их защитные механизмы оказываются слишком слабыми. Но иногда бактерии выживают. Тогда они могут активировать свою самую эффективную противовирусную систему. Они сохраняют часть ДНК вируса в своём генетическом коде, ДНК-архиве “CRISPR”. Здесь она хранится до необходимого момента.
Когда вирус снова атакует, бактерия создает РНК-копию из ДНК архива и
заряжает секретное оружие – белок Cas9. Этот протеин сканирует бактерию на предмет вмешательства вируса, сравнивая каждую часть найденного ДНК с архивом. Когда находится 100% соответствие, он активируется и отрезает ДНК вируса, делая его бесполезным, таким образом защищая бактерию.

Белок Cas9 сканирует ДНК клетки на предмет внедрения вируса и заменяет испорченную часть здоровым фрагментом.
Что характерно, Cas9 очень точен, словно ДНК хирург. Переворот произошел, когда ученые поняли, что система CRISPR программируема – можно просто дать копию ДНК, которую нужно изменить, и поместить систему в живую клетку.
Помимо точности, дешевизны и простоты использования, CRISPR позволяет включать и выключать гены живых клеток и изучать конкретные последовательности ДНК.
Этот метод также работает с любыми клетками, микроорганизмами, растениями, животными или людьми.

Ученые выяснили, что Cas9 можно программировать на любые замены в любой части ДНК – и это открывает практически безграничные возможности для человечества.
Болезням конец?
В 2015-м ученые использовали CRISPR для удаления вируса ВИЧ из клеток пациентов,
и доказали, что это возможно
. Годом позже они провели более амбициозный эксперимент с крысами с вирусом ВИЧ в практически всех их клетках.
Учёные просто ввели CRISPR в их хвосты, и смогли удалить более 50% вируса из клеток по всему телу. Возможно, через несколько десятилетий CRISPR поможет избавиться от ВИЧ и других ретровирусов – вирусов, которые прячутся внутри человеческой ДНК, вроде герпеса. Возможно CRISPR сможет победить нашего худшего врага, рак .
Рак является результатом появления клеток, отказывающихся умирать и продолжающих делиться, попутно прячась от иммунной системы. CRISPR дает нам средство редактировать наши иммунные клетки и делать их лучшими охотниками на раковые клетки.
Возможно через некоторое время лечение от рака будет всего лишь парой уколов с несколькими тысячами ваших собственных клеток, созданных в лаборатории, чтобы вылечить вас навсегда.

Возможно через некоторое время вопрос лечения рака – вопрос пары уколов модифицированных клеток.
Первое клиническое испытание такой терапии на пациентах-людях было одобрено в начале 2016-го в США. Менее чем через месяц китайские ученые объявили, что будут лечить пациентов с раком легких иммунными клетками, модифицированными по этой же технологии, в августе 2016 . Дело быстро набирает обороты.
А еще есть генетические заболевания, тысячи их. Они разнятся от слегка раздражающих до крайне смертельных или приносящих годы страданий. С мощными инструментами вроде CRISPR однажды мы сможем покончить с этим.
Более 3000 генетических заболеваний вызываются единственной заменой в ДНК.
Мы уже создаем модифицированную версию Cas9, которая исправляет такие ошибки и избавляет клетку от заболевания. Через пару десятилетий мы может быть сможем навсегда уничтожить тысячи заболеваний. Однако у всех эти медицинских применений один недостаток – они ограничены одним пациентом и умрут вместе с ним, если мы не используем их на репродуктивных клетках или на ранней стадии развития плода.
CRISPR вероятно будет использоваться куда шире. Например для создания модифицированного человека, спроектированного ребенка. Это принесет плавные но необратимые изменения в человеческом генофонде.
Спроектированные дети
Средства изменения ДНК человеческого плода уже существуют,
но технология находится на раннем этапе развития. Однако, ее применяли уже дважды. В 2015-м и 2016-м эксперименты китайских ученых с человеческими эмбрионами достигли частичного успеха на второй попытке.
Они выявили гигантские трудности в редактировании генов эмбрионов, но множество ученых уже работают над решением этих проблем. Это то же самое, что и компьютеры 70-х: в будущем они станут лучше.
Вне зависимости от ваших взглядов на генную инженерию, она коснётся всех. Модифицированные люди могут изменить геном всего нашего вида, потому что их привитые качества будут переданы их детям, и через поколения медленно распространятся, медленно меняя генофонд человечества. Это начнется постепенно.
Первые спроектированные дети не будут сильно отличаться от нас. Скорее всего, их гены будут изменены для избавления от смертельных наследственных заболеваний.
По мере развития технологий все больше людей начнут думать, что неиспользование генетической модификации неэтично, потому что это обрекает детей
на страдание и смерть, которые можно предотвратить.

Как только первый такой ребенок родится, откроется дверь, которую уже не удастся закрыть. Сначала некоторые черты никто не будет трогать, но по мере роста одобрения технологии и наших знаний о генетическом коде, будет расти будет и соблазн.
Если вы сделаете свое потомство иммунным к болезни Альцгеймера, почему бы вдобавок
не дать им улучшенный метаболизм? Почему бы до кучи не наградить их отличным зрением? Как насчет роста или мускул? Пышных волос? Как насчет дара исключительного интеллекта для вашего ребенка?
Огромные перемены придут как результат накопления личных решений миллионов людей.
Это скользкий склон, и модифицированные люди могут стать новой нормой. Пока генная инженерия становится все более привычной, а наши знания улучшаются, мы можем подойти к искоренению главной причины смертности – старения.

2/3 из примерно 150 000 человек, умерших сегодня, умерли по причинам, связанным со старением.
Сегодня считается, что старение вызывается накоплением повреждений в наших клетках
вроде разрывов ДНК или износа систем, ответственных за исправление этих повреждений.
Но есть также и гены, которые напрямую влияют на наше старение.
Генная инженерия и прочая терапия могли бы остановить или замедлить старение. Возможно даже обратить его вспять.

Типичная реакция на возможность вечной жизни (как и любой другой привычной сейчас, но революционной несколько сотен лет назад технологии).
Вечная жизнь и “люди икс”
Мы знаем, что в природе есть животные, которые не стареют. Может, мы могли бы занять у них пару генов. Некоторые ученые считают что однажды старение будет искоренено. Мы все равно будем умирать, но только не в больнице в 90 лет, а через пару тысяч лет, прожитых в окружении наших любимых.
Вызов огромен и, возможно, цель недостижима, но можно допустить, что люди, живущие сегодня, могут оказаться первыми, кто вкусит плоды анти-возрастной терапии. Возможно, нужно всего лишь убедить смышленого миллиардера в необходимости помочь решить эту большую проблему.
Если смотреть на это шире, мы могли бы решить множество задач с помощью специально измененных людей, например которые могли бы лучше справляться с высококалорийной едой, и избавиться от таких недугов цивилизации как ожирение.
Владея модифицированной иммунной системой с перечнем потенциальных угроз,
мы могли бы стать неуязвимыми для большинства заболеваний, преследующих нас сегодня. Ещё позже мы смогли бы создать людей для длительных космических перелетов и для адаптации к различным условиям на других планетах, что было бы крайне полезно для поддержания нашей жизни во враждебной вселенной.
Несколько щепоток соли
Есть несколько главных препятствий, технологических и этических. Многие почувствуют страх перед миром, где мы отсеиваем несовершенных людей, а потомство выбираем на основе того, что считается здоровым.
Но мы уже живем в таком мире. Тесты на десятки генетических заболеваний или осложнений стали нормой для беременных женщин во многих странах. Часто одно подозрение на генетический дефект может привести к прерыванию беременности.
Возьмем для примера синдром Дауна, один из самых распространенных генетических дефектов: в Европе около 90% беременностей с установленным наличием этого отклонения прерываются.

Генетический отбор в действии: уже сейчас синдром Дауна диагностируется на ранней стадии развития эмбриона и 90% беременности с этим диагнозом прерывается.
Решение о прерывании беременности является очень личным, но важно понимать, что мы уже сегодня отбираем людей, основываясь на состоянии здоровья. Нет смысла притворяться, что это изменится, поэтому нам необходимо действовать осторожно и этично, несмотря на растущую свободу выбора благодаря дальнейшему развитию технологий.
Однако, все это перспективы отдаленного будущего. Несмотря на мощность CRISPR, метод не лишен недостатков. Могут случиться ошибки при редактировании, неизвестные ошибки могут произойти в любой части ДНК и остаться незамеченными.
Изменение гена может достичь нужного результата и вылечить от заболевания, но вместе с этим спровоцировать нежелательные изменения. Мы попросту недостаточно знаем о сложных взаимосвязях наших генов, чтобы избежать непредсказуемых последствий.
Работа над точностью и методами наблюдения очень важна в предстоящих клинических испытаниях. И раз уж мы обсудили возможное светлое будущее, также стоит упомянуть и более мрачное видение. Представьте, что может страна вроде Северной Кореи сделать с таким уровнем технологий?

Важно, чтобы технология генной модификации не попала в руки тоталитарным режимам, которые гипотетически могут использовать ее во вред человечеству – например, создать армию генетически модифицированных солдат.
Может она навечно продлить свое правление с помощью принудительной инженерии? Что остановит тоталитарный режим от создания армии модифицированных суперсолдат?
Ведь это в теории возможно. Сценарии вроде этого лежат в далеком будущем, если они вообще возможны, но подтверждение работоспособности концепции такой инженерии уже существует. Технология и правда настолько могущественна.
Подобное может стать поводом для запрета инженерии и связанных с ней исследований, но это определенно было бы ошибкой. Запрет на генную инженерию человека только приведёт науку в области с такими правилами и законами, с которыми нам было бы не по себе. Только участвуя в процессе, мы сможем быть уверены, что исследование ведется с осторожностью, разумом, контролем и прозрачностью.

Мы можем исследовать и внедрять в человека любые генные модификации.
Заключение
Чувствуете беспокойство? Почти в каждом из нас есть какое-то несовершенство. Позволили бы нам существовать в подобном новом мире? Технология несколько устрашает, но нам есть что выиграть, да и генная инженерия может быть очередной ступенью в эволюции разумных видов жизни.
Возможно мы покончим с болезнями, увеличим продолжительность жизни на века и отправимся к звездам. Не стоит мелко мыслить, говоря о такой теме. Каким бы ни было ваше мнение о генной инженерии, будущее наступает несмотря ни на что.
То, что раньше было научной фантастикой, вскоре станет нашей новой реальностью.
Реальностью, полной возможностей и препятствий.
Вы можете также посмотреть непосредственно само видео:
Может показаться, что ДНК - главный центр молекулы, без которой ее жизнь невозможна. На самом деле ДНК - достаточно чувствительная сложная молекула, которая сама способна быстро изменяться и проявлять особенные свойства. На нее оказывают влияние как наши мысли и намерения, так и факторы воздействия физического и химического характера.
Сложные цепочки генетических кодов, каждое звено которых может перестать работать или активизироваться в любую минуту - вот что представляет собой сосредоточение генетического материала человека. Кроме того, спирали генов способны проявлять невероятные свойства и помогать сохранять энергию невероятно длительное время. Но как такое возможно и как можно настроить свой организм на исцеления путем влияния на ДНК?
Световая ловушка
Фотоны света не задерживаются, а постоянно рассеиваются. В растениях энергия света преобразуется в молекулы питательных веществ, а в организме человека для улавливания фотонов света может служить спиралевидная молекула ДНК. Это доказано в эксперименте с помещением ДНК в кварцевый контейнер и облучением его светом. Интересно, что сам свет приобретал также спиралевидную структуру и мог храниться в течение месяца даже после того, как молекулу ДНК удалили из контейнера. Такое преобразование и хранение световой энергии доступно только спиралевидным молекулам, которые ответственны за передачу генетической информации.
Самостоятельное исцеление
Многие люди считают, что наследственность играет основную роль в состоянии здоровья. На самом деле экспериментальные данные о значении позитивного мышления в управлении ДНК говорят о том, что гены определяют нас всего лишь отчасти, в остальном же человек сам отвечает за собственные болезни и склонности. При стрессах, раздражении, постоянных переживаниях гены перестают работать нормально, возникают предпосылки для развития болезней. Патологии могут затрагивать абсолютно любые органы и ткани, но все начинается с мышления и саморазрушающих механизмов воздействия сознания на спиралевидные молекулы.
Источником энергии для оздоровления клеточных молекул является любовь. Это способ направленного целительного омоложения клеток, предотвращения их старения и разрушения. Любовь позволяет усиливать позитивную энергию и делать мысли более сильными. Без любви организм не может развиваться нормально. Это доказывают экспериментальные наблюдения, когда дети не могу полноценно развиваться, если им не хватает родительской ласки и любви. Доказано, например, что дети из приютов чаще страдают от аутизма, чем малыши, о которых заботятся родители.
Мыслительные преобразовании
Воздействовать на структурные изменения в ДНК можно на расстоянии посредством намерения.
Если человек осознанно концентрируется на хороших мыслях, а его мозг начинает излучать гармоничные волны, но спирали ДНК начинают преобразовываться. Причем, если человек воздействует позитивными мыслями и намерениями, то изменения приводят к исцеляющим преобразованиям, а если в мыслях присутствует направленный гнев, злоба, раздражение, то ДНК настраиваются на волну умирания. Все дело в том, что мозг начинает преобразовывать мысли в потоки энергии, которые воспринимаются и интерпретируются ДНК как сигналы к восстановлению организма, или, наоборот, к самоуничтожению.
По данным экспериментов изменения в структуре ДНК, помещенной в изолированную пробирку с нейтральной средой, при отсутствии мыслительного воздействия практически не имели место. Зато при сосредоточении мыслей именно на пробирке с ДНК начинались изменения в 10% участков молекулы, которая несет генетическую информацию. Вот как работают целители. Они способны преобразовать позитивные мысли и настрои в энергию мозговых волн. Именно такие волны дают клеткам организма сигналы о необходимости исцеления органов и систем.
У однояйцовых близнецов одинаковый набор генов. Но почему-то один не вылезает из болезней, а другой ни разу не чихнул. Получается, наше здоровье зависит не только от того, что мы наследуем от родителей, но и от других факторов? Наука эпигенетика доказала: человек может изменить то, что ему "на роду написано", то есть свою ДНК. Каким же образом?
Если человек будем придерживаться сбалансированной диеты, забудет про вредные привычки и приобретет полезные, он не только сможет изменить свою жизненную программу, записанную в собственном ДНК, но и передаст потомкам здоровые гены, которые продлят годы детям и внукам.
Чеснок запускает гены
Первый и главный — еда. В принципе, каждый из продуктов может влиять на работу генов. Но есть некоторые, полезность которых ученые уже доказали на все 100 процентов.
Среди них — зеленый чай. В зеленом чае есть вещества катехины (epigallocatechin-3-gallate, epicatechin, epicatechin-3-gallate, epigallocatechin), им по силам подавлять гены, способствующие онкологическим заболеваниям, и активировать те гены, которые умеют сражаться с опухолями. Чтобы поддерживать свое ДНК в боеготовности "антирак", достаточно выпивать ежедневно 2-3 небольшие чашки зеленого чая. Особо полезен зеленый чай женщинам, среди родственниц которых есть больные опухолями молочной железы.
Другой продукт — чеснок. В чесноке работают другие соединения — diallyl sulfide, diallyl disulfide, diallyl trisulfide. Надо съедать 2-3 зубчика чеснока в день, чтобы запустить гены, которые заведуют не только процессами гибели клеток, дающих метастазы, но и сражаются со старостью, продляют жизнь.
Третья панацея — соя. В сое содержатся изофлавоноиды (genistein, daidzein) — действенное противоопухолевое средство при раке груди, простаты, гортани, толстой кишки и лейкемии. Ученые советуют употреблять сою в БАДах и придерживаться дозировки, указанной на упаковках.
Четвертый борец за здоровые гены — виноград и продукты из него (сок и вино). Гроздь винограда темных сортов (это 120 г виноградного сока или 100 г сухого красного вина), добавленная в ежедневное меню, обеспечит организм веществом resveratrol, меняющим гены.
В рацион, который понравится добрым генам, стоит включить 100 г темно-красных помидоров (вещество lycopene) с добавлением оливкового масла. Помидоров надо есть вчетверо больше, если в роду есть онкобольные.
Еще один овощ, который добрым словом вспомнят ваши наследники, — капуста брокколи (вещество indole-3-carbinol). 100 г брокколи — каждому, 300 г — при риске рака.
Обязательно надо есть орехи, рыбу, яйца и грибы — они обеспечивают организм микроэлементами селеном и цинком, которые тоже меняют ДНК.
Тучная конституция закреплялось в геноме
Работа генов зависит от режима питания. Диета должна быть низкокалорийной (не более 2 тысяч ккал в сутки). Она отодвигает старение человека, гарантирует долголетие его детям и внукам. Эпидемию ожирения, разразившуюся сегодня, тоже объясняет эпигенетика: мы становимся все полнее, поскольку переедают наши мамы до беременности и во время нее. Это подтверждают опыты, проведенные на животных: перекормленные мыши каждый раз производили еще более тучное потомство, и подобная конституция закреплялось в геноме.
Генам нравится, когда их хозяин поддерживает себя в хорошей физической форме. Ученые определили, что регулярные занятия в течение 45 дней на обычном велотренажере активируют около 500 генов! А если заниматься регулярно и дальше — то можно изменить к лучшему еще больше генов.
Про вредные привычки писано-переписано. Но влияние сигарет, спиртного и наркотиков непосредственно на гены доказано лишь недавно. Оказывается, более 150 участков ДНК у хронических алкоголиков получают ненормальную активность. Результат: алкоголик не может сосредоточиться, ничего не запоминает, не может обуздать свои эмоции. Но самое печальное — он передает больные гены потомству.
И около 120 генов остаются измененными даже спустя 10 лет после отказа от сигарет. И опять среди них есть и самые важные гены, контролирующие деление клетки. Результат — рак у курильщика. Но тут есть повод для оптимизма: гены можно исправить, и чем меньше стаж пристрастия к , тем скорее это можно сделать.
На гены влияют и эмоции, как положительные, так и отрицательные, полученные дома, в семье, на работе.
Ну и, наконец, экологическая ситуация, в которой живет человек. Очевидно, что промышленные выбросы, автомобильные выхлопы, нитраты в еде, загрязненная вода тоже приводят к поломкам в генах.
Хотите жить дольше? Желаете здоровья своим детям и внукам? Тогда проявляйте заботу о своих генах.
Теперь вы знаете, как это делать?
Изменение ДНК человека которое передается будущим поколениям уже давно считается этически закрытым и запрещенным во многих странах. Ученые сообщают, что они используют новые инструменты для ремонта болезнетворных генов в эмбрионах человека. Хотя исследователи используют дефектные эмбрионы и не собираются имплантировать их в матку женщины, работа вызывает опасение.
Изменение ДНК человеческих яйцеклеток, спермы или эмбрионов известно как герминативное изменение. Многие ученые призывают к мораторию на пересмотр клинических эмбрионов, редактирование зародышевой линии человека и многие считают, что этот вид научной деятельности должен быть запрещен.
Однако, редактирование ДНК человеческого эмбриона может быть этически допустимо, чтобы предотвратить болезнь у ребенка, но только в редких случаях и с гарантиями. Эти ситуации могут быть ограниченно введены для пар, когда они оба имеют серьезные генетические заболевания и для кого редактирование эмбриона действительно последний разумный вариант, если они хотят иметь здорового ребенка.
Опасность преднамеренного изменения генов
Ученые считают, что редактирование эмбриона человека может быть приемлемым, чтобы предотвратить ребенка от наследования серьезных генетических заболеваний, но только при соблюдении определенной техники безопасности и этических критериев. Например, пара не может иметь “разумные альтернативы”, такие как возможность выбора здоровых эмбрионов для экстракорпорального оплодотворения (ЭКО) или с помощью пренатальных тестов и аборта плода с болезнью. Другая ситуация, которая может удовлетворить критериям, если оба родителя имеют одинаковые заболевания, такие как, например, кистозный фиброз.
Ученые предупреждают о необходимости строгого государственного надзора, чтобы предотвратить использование редактирования зародышевой линии для других целей, например, чтобы дать ребенку желаемые, отличительные от остальных черты.
Редактирование генов в клетках пациентов, которые не наследуются, клинические испытания уже ведутся для борьбы с ВИЧ, гемофилией и лейкозом. Считается, что существующие регуляторные системы для генной терапии которые являются достаточными для проведения таких работ.
Редактирование генома не должно быть для повышения потенции, повышения у здорового человека мышечной силы или снижения уровня холестерина.
Редактирование генов человеческой зародышевой линии или модификация зародышевой линии человека означает преднамеренное изменение генов передающееся детям и будущим поколениям.
Другими словами, создание генно-модифицированных людей . Модификация зародышевой линии человека на протяжении многих лет считается запретной темой в связи с безопасностью и социальными причинами. Это формально запрещено в более чем 40 странах.
Опыты по созданию генно-модифицированных людей и наука евгеника
Однако, в последние годы, по новым методам генной инженерии, проводились опыты с человеческими эмбрионами. Для исследований использовались гены и человеческие эмбрионы связанные с бета-заболеванием крови – талассемией. Эксперименты были в основном безуспешными. Но инструменты редактирования генов совершенствуются в лабораториях по всему миру и ожидается, что они позволят легче, дешевле и более точнее редактировать или удалять гены, чем когда-либо прежде. Современные пока теоретические способы редактирования генома позволят ученым вставлять, удалять и подправлять ДНК с получением положительных результатов. Это открывает перспективу лечения некоторых заболеваний, таких как серповидно-клеточные заболевания, муковисцидоз и определенные виды рака.
Селекция применительно к человеку – евгеника
Редактирование генов человеческих эмбрионов или направление евгеника приводит к созданию генетически модифицированных очень разных людей. Это вызывает серьезную безопасность в связи с социальными и этическими проблемами. Они варьируются от перспективы необратимого вреда для здоровья будущих детей и поколений до открывания дверей к новым формам социального неравенства, дискриминации и конфликтов и новой эре евгеники.
Наука евгеника по селекции человека попала в середине прошлого века как наука нацистского направления.
Ученым не разрешено вносить изменения в ДНК человека, который передается последующим поколениям. Такой новаторский шаг науки евгеники следует рассматривать лишь после дополнительных исследований, после чего изменения могут быть проведены в условиях жестких ограничений. Такие работы должны быть запрещены, чтобы предотвратить серьезные заболевания и инвалидности.
Изменчивость вызванную изменением генов называют ещё мутациями.
Это давнее табу на внесение изменений в гены человеческой спермы, яйцеклеток или эмбрионов, потому что такие изменения будут унаследованы будущими поколениями. Это табу отчасти из-за опасений, что ошибки могут непреднамеренно создать новые искусственные болезни, которые потом могут стать постоянной частью человеческого генофонда.
Другая проблема заключается в том, что этот вид может быть использован для генетической модификации для немедицинских причин. Например, ученые теоретически могут попытаться создать конструктор детей, в которых родители пытаются выбрать черты характера своих детей, чтобы сделать их умнее, выше, лучшими спортсменами или с другими якобы необходимыми атрибутами.
Ничего подобного в настоящее время не возможно. Но даже перспектива вызывает опасения ученых существенно изменить ход эволюции и создания людей, которые считаются генетически улучшенными, придумывать какие антиутопии будущего, описанные в фильмах и книгах.
Любая попытка создания младенцев от спермы, яйцеклеток или эмбрионов, которые имеют свои ДНК и пытаться редактировать можно только при очень тщательно контролируемых условиях и только для предотвращения разрушительного заболевания.
Это может быть сложно в дальнейшем провести грань между использованием генного редактирования, чтобы предотвратить или обработать заболевание и использовать его для повышения возможностей человека.
Например, если ученым удается выяснить, что изменения генов повышают мыслительные способности, чтобы отбиваться от деменции при болезни Альцгеймера, то это можно считать профилактической медициной. Если просто кардинально улучшить память здорового человека, то это уже не медицинское направление.
Когда разрешено изменять ДНК
Возможность редактирования генов и может быть использована для лечения многих заболеваний и, возможно, даже предотвратить многие разрушительные расстройства от происходящих в первую очередь путем редактирования из генетических мутаций в сперме, яйцеклетке и эмбрионе. Некоторые потенциальные изменения могли бы предотвратить широкий спектр заболеваний, включая рак молочной железы, болезнь Тея-Сакса, серповидноклеточную анемию, кистозный фиброз и болезнь Хантингтона.
Клинические испытания редактирования генов должны быть разрешены, если:
- нет “разумной альтернативы”, чтобы не допустить “серьезного заболевания”
- убедительно доказано, что гены, будучи отредактированы устраняют причину заболевания
- изменения направлены лишь на преобразование таких генов которые связаны с обычным состоянием здоровья
- проведена достаточная предварительная исследовательская работа на тему рисков и потенциальных выгод для здоровья
- постоянный, строгий надзор для изучения влияния процедуры на здоровье и безопасность участников, а также долгосрочные комплексные планы
- есть максимальная прозрачность в соответствии с конфиденциальностью пациента и ведется переоценка, здоровья, социальные выгоды и риски
- есть надежные надзорные механизмы, чтобы предотвратить расширение серьезной болезни или состояния.
Сторонники редактирования зародышевой линии человека, утверждают, что это могло бы потенциально уменьшить или даже устранить, возникновение многих серьезных генетических заболеваний уменьшили бы человеческие страдания во всем мире. Оппоненты говорят, что изменения человеческих эмбрионов опасно и противоестественно, и не учитывает согласие будущих поколений.
Дискуссия по изменению зародыша человека
 Начнем с возражением о том, что изменение зародыша – это противоестественно или играть против Бога.
Начнем с возражением о том, что изменение зародыша – это противоестественно или играть против Бога.
Этот аргумент основывается на предпосылке, что естественное по своей сути хорошее.
Но болезни являются естественными и люди миллионами заболевают и умирают преждевременно-все совершенно естественно. Если бы мы только охраняли природные существа и природные явления, мы бы не смогли использовать антибиотики, чтобы убить бактерии или иначе занимались бы медициной или боролись с засухой, голодом, мором. Система здравоохранения ведется в каждой развитой стране и может быть справедливо охарактеризована как часть всеобъемлющей попытки сорвать ход природы. Что естественно не является ни хорошим, ни плохим. Природные вещества или естественные методы лечения лучше, если они, конечно, возможны.
Приводит к важному моменту в истории медицины и редактирование генома и представляет перспективные начинания науки на благо всего человечества.
Вмешательство в геном человека допущено только в профилактических, диагностических или терапевтических целях и без внесения модификаций для потомков.
Стремительный прогресс в области генетики так называемый “дизайнер младенцев” увеличивает необходимость биоэтики для широкой общественной и ведении дискуссии о силе науки. Наука способна генетически модифицировать человеческие эмбрионы в лаборатории, чтобы контролировать унаследованные черты, такие как внешний вид и интеллект.
По состоянию на сейчас многие страны подписали международную Конвенцию, запрещающую этот вид редактирования генов и изменение ДНК.
Дженнифер Дудна – известная ученая из США, труды которой в основном посвящены структурной биологии и биохимии. Дженнифер лауреатка многих престижных премий, в 1985 году получила степень бакалавра, а уже в 89 году стала доктором философии в Гарвардском университете. С 2002 года работает в Калифорнийском университете в Беркли. Широкую известность получила как исследователь РНК-интерференции и CRISPR. Исследования по Cas9 проводила вместе с Эммануэль Шарпантье.
00:12
Несколько лет назад мы с моей коллегой Эммануэль Шарпентье изобрели новую технологию редактирования геномов. Она называется CRISPR-Cas9. Технология CRISPR позволяет учёным вносить изменения в ДНК внутри клеток, что может дать нам возможность вылечивать генетические заболевания.
00:31
Возможно, вам будет интересно узнать, что технология CRISPR возникла в рамках проекта фундаментальных исследований, целью которого было выяснение того, как бактерии борются с вирусными инфекциями. Бактериям приходится сталкиваться с вирусами в среде своего обитания, и вирусную инфекцию можно представить как тикающую бомбу замедленного действия: у бактерии есть всего несколько минут, чтобы её обезвредить до того как бактерия будет разрушена. В клетках многих бактерий существует адаптивная иммунная система - CRISPR, позволяющая им выявлять и разрушать вирусную ДНК.
01:04
В состав системы CRISPR входит белок Cas9, который способен искать, расщеплять и в конечном итоге уничтожать вирусную ДНК особым способом. И именно в ходе нашего исследования по изучению активности этого белка, Cas9, мы поняли, что можем использовать его активность в генно-инженерной технологии, которая позволит учёным удалять и вставлять фрагменты ДНК внутрь клеток с невероятной точностью, что позволило бы делать то, что ранее было просто невозможно.
01:42
Технология CRISPR уже используется для изменения ДНК в клетках мышей и обезьян, а также других организмов. Недавно китайские учёные показали, что им удалось использовать технологию CRISPR даже для изменения генов эмбрионов человека. Учёные из Филадельфии показали возможность применения CRISPR для удаления ДНК интегрировавшегося вируса ВИЧ из инфицированных клеток человека.
02:09
Возможность осуществлять редактирование генома таким образом также вызывает различные этические вопросы, которые следует иметь в виду, потому что технологию можно применять не только к клеткам взрослых, но также и к эмбрионам разных организмов, в том числе и нашего вида. Таким образом, вместе с коллегами мы начали международное обсуждение изобретённой нами технологии, чтобы иметь возможность учесть все этические и общественные проблемы, связанные с подобными технологиями.
02:39
А сейчас я хочу рассказать вам, что такое технология CRISPR, что она позволяет делать, на каком мы сейчас этапе и почему я считаю, что нам нужно с осторожностью продвигаться вперёд по пути применения этой технологии.
02:54
Когда вирусы инфицируют клетку, они впрыскивают свою ДНК. И внутри бактерии система CRISPR позволяет выдернуть эту ДНК из вируса и вставить её маленькие фрагменты в хромосому - в ДНК бактерии. И эти фрагменты вирусной ДНК вставляются в область, называемую CRISPR. CRISPR означает «короткие палиндромные повторы, регулярно расположенные группами». (Смех)
03:24
Длинновато. Теперь вы понимаете, почему мы используем акроним CRISPR. Это механизм, позволяющий клеткам регистрировать с течением времени вирусы, которые их заражали. И важно отметить, что эти фрагменты ДНК передаются потомкам клеток, так что клетки защищены от вирусов не в течение одного поколения, а в течение многих поколений клеток. Это позволяет клеткам сохранять «записи» об инфекции, и как говорит мой коллега Блейк Виденхефт, локус CRISPR - это фактически карточка генетической вакцинации клеток. После встраивания этих фрагментов ДНК в бактериальную хромосому клетка делает маленькую копию в виде молекулы, называемой РНК, на этом рисунке она оранжевая, и это точный отпечаток вирусной ДНК. РНК - химическая «кузина» ДНК, что позволяет ей взаимодействовать с молекулами ДНК, имеющими подходящую для неё последовательность.
04:24
Итак, эти маленькие фрагменты РНК, образованные с локуса CRISPR, ассоциируют, связываются с белком под названием Cas9, на этом рисунке он белый, и образуется комплекс, который выполняет в клетке функции часового. Он просматривает всю ДНК в клетке, чтобы найти участки, соответствующие последовательностям связанных с ним РНК. И когда эти участки найдены, как можно видеть на рисунке, где ДНК - это синяя молекула, этот комплекс связывается с этой ДНК и даёт белку Cas9 разрезать вирусную ДНК. Он очень точно вносит разрыв. Мы можем рассматривать этого часового, комплекс белка Cas9 и РНК, как пару ножниц, которые могут разрезать ДНК, - он делает двуцепочечный разрыв в спирали ДНК. И важно, что этот комплекс можно запрограммировать, например, можно его запрограммировать узнавать нужные последовательности ДНК и разрезать ДНК в на этом участке.
05:26
Как я собираюсь вам рассказать, мы поняли, что эту активность можно использовать в генной инженерии, чтобы позволить клеткам вносить очень точные изменения в ДНК на участке, где был сделан данный разрез. Это примерно как использование программы, обрабатывающей слова, для исправления опечаток в документе.
05:48
Мы смогли предположить, что систему CRISPR можно использовать в геномной инженерии, поскольку клетки способны находить разорванную ДНК и восстанавливать её. Итак, когда клетка растения или животного находит двуцепочечный разрыв в своей ДНК, она способна его устранить, либо соединяя разорванные концы ДНК, внося незначительное изменение в последовательность в этом месте, либо она может устранить разрыв, вставив новый участок ДНК в место разрыва. Таким образом, если мы можем вносить двуцепочечные разрывы в ДНК в строго определённых местах, мы можем заставить клетки восстанавливать эти разрывы, при этом либо разрушая генетическую информацию, либо внося новую. И если бы мы смогли запрограммировать технологию CRISPR таким образом, чтобы разрыв в ДНК вносился в положении мутации или рядом с мутацией, вызывающей, например, муковисцидоз, мы могли бы заставить клетки исправить эту мутацию.
06:51
Вообще-то, геномная инженерия - не новая область, она развивается с 1970-х годов. У нас есть технологии для секвенирования ДНК, для копирования ДНК, даже для манипуляций с ДНК. И это весьма многообещающие технологии, но проблема в том, что они были либо неэффективны, либо слишком сложны в использовании, поэтому большинство учёных не могли использовать их в своих лабораториях или применять в клинических условиях. Таким образом, существовала потребность в такой технологии как CRISPR, потому что она относительно проста в использовании. Старые технологии геномной инженерии можно представить себе как необходимость перемонтировать ваш компьютер каждый раз, когда вы хотите запустить новую программу, тогда как технология CRISPR - это что-то вроде программного обеспечения для генома: мы легко можем её программировать, используя маленькие фрагменты РНК.
07:53
Как только сделан двуцепочечный разрыв, мы можем вызвать процесс восстановления и тем самым, возможно, достичь поразительных результатов, например, исправлять мутации, вызывающие серповидноклеточную анемию или болезнь Хантингтона. Лично я считаю, что первые случаи применения технологии CRISPR будут связаны с кровью, где относительно просто доставлять этот инструмент внутрь клеток, по сравнению с плотными тканями.
08:22
Прямо сейчас во многих проводимых работах метод применяют в животных моделях болезней человека, например, на мышах. Технологию используют для внесения очень точных изменений, что позволяет нам изучать то, как эти изменения клеточной ДНК влияют либо на ткань, либо, как здесь, на целый организм.
08:42
В этом примере технологию CRISPR использовали для разрушения гена путём внесения небольшого изменения в ДНК в гене, который отвечает за чёрную окраску шерсти этих мышей. Представьте, эти белые мышата отличаются от своих окрашенных братьев и сестёр всего только небольшим изменением одного гена во всём геноме, а в остальном они абсолютно нормальны. И когда мы секвенируем ДНК этих животных, то обнаруживаем, что изменение в ДНК произошло именно в том месте, где мы планировали, используя технологию CRISPR.
09:18
Также проводятся эксперименты и на других животных, у которых удобно создавать модели болезней человека, например, на обезьянах. И в этом случае мы обнаруживаем, что эти системы можно использовать для тестирования применения данной технологии к определённым тканям, например, для выяснения того, как доставлять инструмент CRISPR в клетки. Мы также хотим расширить наше понимание того, как можно контролировать способ восстановления ДНК после её разрыва, и выяснить, как можно контролировать и ограничивать нецелевое воздействие, или непреднамеренные эффекты, при использовании этой технологии.
09:55
Я полагаю, что мы станем свидетелями использования данной технологии в клинике, разумеется, у взрослых пациентов, в течение следующих 10 лет. Мне кажется вероятным, что за этот период будут проведены клинические исследования и, возможно, даже одобрены методы терапии, что очень воодушевляет. И благодаря этому воодушевлению, которое вызывает технология, к ней проявляют огромный интерес стартап-компании, созданные для того, чтобы превратить технологию CRISPR в коммерческий продукт, а также многие венчурные капиталисты,
10:26
инвестирующие в такие компании. Но мы также должны учитывать, что технологию CRISPR можно использовать для улучшения характеристик. Представьте, что мы могли бы попробовать конструировать людей, обладающих улучшенными характеристиками, например, более прочными костями, или меньшей склонностью к сердечно-сосудистым заболеваниям, или даже обладающих свойствами, которые, возможно, показались бы нам желательными, такими как другой цвет глаз или более высокий рост, что-то вроде этого. Если хотите, это «дизайнерские люди». Сейчас практически отсутствует генетическая информация, позволяющая понять, какие гены отвечают за эти признаки. Но важно понимать, что технология CRISPR дала нам инструмент для внесения таких изменений,
11:13
как только эти знания станут нам доступны. Это поднимает ряд этических вопросов, которые мы должны тщательно рассмотреть. И именно поэтому мы с коллегами призвали учёных всего мира сделать паузу в любых клинических применениях технологии CRISPR у эмбрионов человека, чтобы у нас было время тщательно рассмотреть все возможные последствия этого. И у нас есть важный прецедент для того, чтобы объявить такую паузу: в 1970-х годах учёные объединились для провозглашения моратория на использование молекулярного клонирования,
11:47
пока не будет тщательно проверена и подтверждена безопасность этой технологии. Так что пока генная инженерия людей откладывается, но это уже не научная фантастика. Созданные генной инженерией животные и растения уже существуют. И это накладывает на всех нас большую ответственность и необходимость учитывать как нежелательные последствия, так и роль преднамеренного влияния этого научного прорыва.
12:21
Спасибо!
12:22
(Аплодисменты) (Аплодисменты закончились)
Бруно Джуссани: Дженнифер, эта технология может иметь огромные последствия, как вы подчёркивали. Мы очень уважаем вашу позицию по объявлению паузы, или моратория, или карантина. У всего этого, конечно, есть терапевтические последствия, но есть и не связанные с лечением, и, по-видимому, именно они наиболее сильно притягивают интерес, особенно в СМИ. Вот один из последних выпусков журнала Economist: «Редактирование человечества». Здесь рассказывается только об улучшении свойств, не о лечении. Какую реакцию вы получили в марте от своих коллег в научном сообществе, когда попросили или предложили сделать паузу и задуматься обо всём этом?
Дженнифер Дудна: Мне кажется, коллеги были рады возможности открыто это обсудить. Интересно, что когда я разговаривала об этом с людьми, мои коллеги-учёные и не только высказывали самые разные точки зрения на этот счёт. Очевидно, что эта тема требует тщательного рассмотрения и обсуждения.
БДж: В декабре будет большая встреча, которую вы с коллегами созываете вместе с Национальной академией наук и другими. Чего именно вы ожидаете от этой встречи, с практической точки зрения?
ДжД : Я надеюсь, что будут обнародованы точки зрения многих людей и заинтересованных сторон, желающих ответственно обдумать использование этой технологии. Возможно, достигнуть консенсуса не удастся, но я полагаю, что мы должны по крайней мере понять, с какими проблемами столкнёмся в будущем.
БДж: Ваши коллеги, например, Джордж Чёрч из Гарварда, говорят: «Этические проблемы в основном являются вопросом безопасности. Мы снова и снова проводим тесты на животных, в лабораториях, и когда чувствуем, что опасности нет, переходим на человека». Это другой подход: мы должны использовать эту возможность и не должны останавливаться. Может ли это вызвать раскол в научном сообществе? То есть мы увидим, что часть людей отступят, потому что сомневаются в этичности, а другие просто пойдут вперёд, так как в некоторых странах контроль слабый или его вообще нет.
ДжД : Мне кажется, на любую новую технологию, особенно такую как эта, будет несколько разных точек зрения, и я думаю, что это абсолютно понятно. Полагаю, в конце концов эту технологию будут использовать для конструирования генома человека, но мне кажется, что делать это без тщательного рассмотрения и обсуждения рисков и возможных осложнений было бы безответственно.
БДж: Есть много технологий и других областей науки, которые развиваются по экспоненте, фактически как в вашей области. Я имею в виду искусственный интеллект, автономных роботов и так далее. Нигде, как мне кажется, кроме области автономных военных роботов, никто не инициировал аналогичную дискуссию в этих областях, призвав к мораторию. Не считаете ли вы, что ваша дискуссия может стать примером для других областей?
ДжД: Мне кажется, учёным сложно покидать лабораторию. Если говорить обо мне, мне не очень комфортно это делать. Но я действительно считаю, что раз я участвую в разработке этого, то данный факт накладывает на меня и моих коллег ответственность. И я бы сказала, что надеюсь, что другие технологии будут рассматриваться так же, как мы хотели бы рассматривать нечто, способное оказывать влияние в других областях, отличных от биологии.
15:44
БДж:
Дженнифер, спасибо за то, что пришли на TED.
ДжД : Спасибо!
Читайте на Зожнике.