В съответствие с новата класификация на туморите на лимфоидната тъкан (СЗО 2008), HIV-асоциираните лимфоми са разделени в отделна подгрупа "Лимфопролиферативни заболявания, свързани с имунодефицит". В резултат на изследването беше установено, че вирусът на човешката имунна недостатъчност (ХИВ) значително повишава риска от развитие на хронични лимфопролиферативни заболявания, като неходжкинови лимфоми (НХЛ) и лимфом на Ходжкин. (LH). Епидемиологично е доказано, че ХИВ-инфектирани пациентихарактерно е 60-200-кратно увеличение на честотата на НХЛ. Увеличението на броя на пациентите с НХЛ сред ХИВ-инфектираните е 5,6% годишно, в сравнение с 0,015% в общата популация. Рискът от НХЛ или първичен лимфом на централната нервна система (ЦНС) при HIV-инфектирани лица е силно свързан с броя на CD4. Едно проучване установи, че NHL се е увеличил от 15,6 на 253,8 на 10 000 човеко-години, а първичният лимфом на ЦНС от 2 на 93,9 на 10 000 човеко-години при пациенти с брой на CD4 >350 клетки/µl в сравнение с пациенти с<50 клеток/мкл CD4 соответственно .
Освен това е доказано, че пациентите с по-нисък брой на CD4 най-често се диагностицират с първичен лимфом на ЦНС и първичен ексудатен лимфом (PLE), докато в същото време пациентите, инфектирани с HIV, с повече високо ниво CD4 клетки разкриват HL и лимфом на Бъркит (BL).
Повечето HIV-свързани лимфоидни тумори, според онтогенезата на клетките на лимфоидната тъкан, принадлежат към дифузен голям В-клетъчен лимфом (DLBCL), който включва също първичен лимфом на ЦНС. АН при ХИВ-асоциирани пациенти е 30-40%. PLE, плазмобластичен лимфом и HL се диагностицират много по-рядко. Други подвидове лимфоми, като фоликуларен лимфом и периферен Т-клетъчен лимфом, също могат да се развият в тази група, но са редки.
Патогенеза на ХИВ-асоциираните лимфоми
Патогенезата на асоциирания с ХИВ лимфом включва сложно взаимодействие на биологични фактори като хронична антигенна стимулация, коинфекция с онкогенни вируси, генетични аномалии и нарушена регулация на цитокини.
Хроничната антигенна стимулация, която е свързана с ХИВ инфекция, може първоначално да доведе до увеличаване на броя на поликлоналните В клетки и вероятно допълнително да допринесе за появата на моноклонални В клетки.
Наскоро беше отбелязано увеличаване на броя на циркулиращите свободни леки вериги на имуноглобулин при пациенти с повишен риск от развитие на HIV-асоцииран лимфом, който може да действа като маркер за поликлонална В-клетъчна активация. Настоящите проучвания за идентифициране на свободни имуноглобулинови леки вериги могат да бъдат полезни при определяне дали инфектираните с ХИВ лица са изложени на повишен риск от развитие на лимфом.
Най-често в приблизително 40% от случаите на HIV-асоциирани лимфоми се открива онкогенният вирус на Epstein-Barr (EBV). Почти всички пациенти с първичен ЦНС и HL лимфом имат EBV. В повечето случаи на асоциирана с HIV PLE се отбелязва асоциацията на 2 онкогенни вируса: EBV и херпесен вирус тип 8 (човешки херпесен вирус - HHV-8), който присъства при почти всички пациенти. EBV се открива при 30–50% от асоциираните с HIV LB и при 50% от случаите на плазмобластен лимфом (Таблица 1). EBV-позитивните HIV-асоциирани лимфоми често експресират латентен мембранен протеин 1, който активира клетъчната пролиферация чрез активиране на NF-kB пътя и индуциране на свръхекспресия BCL2,по този начин блокира апоптозата на туморните В-клетки, насърчавайки тяхното оцеляване.
Маса 1.Асоциация на онкогенни вируси при пациенти с HIV-лимфоми
| Хистологичен вариант | VEB+ | HHV-8 |
| DVKKL | ||
| Центрорегионален | 30% | 0 |
| имунобластичен | 80–90% | 0 |
| Плазмобластни | >50% | 80% |
| PLE | 100% | 100 |
| LB | 30–50% | 0 |
| Първичен лимфом на ЦНС | 100% | 0 |
| LH | 80–100% | 0 |
Повишените нива на цитокини като IL-6, IL-10, фактор на туморна некроза-β заедно с честите аберантни хипермутации на соматични имуноглобулинови гени показват ролята на имунната стимулация в лимфонкогенезата при HIV-инфектирани пациенти.
Полиморфизмът на хемокиновите пътища също влияе върху риска от развитие на HIV-свързани лимфоми. Например при HIV инфекция 3 ՛ А-вариант фактор 1 на стромални производни клеткисе удвоява, което увеличава 4 пъти риска от НХЛ съответно при хетерозиготи и хомозиготи.
Молекулярно-генетични характеристики на HIV-свързани лимфоми
В резултат на изследването, цяла линиягенетични аномалии при HIV-асоциирани лимфоми. A. Carbone (2003) доказва, че LB е свързано с активирането MYCген. Интересното е, че около 20% от заразените с ХИВ пациенти с DLBCL също имат MYC-транслокация. При пациенти с HIV-асоциирани лимфоми BCL6 мутацията се среща в 20% от случаите с центробластен DLBCL и в 60% с PLE.
Гените, свързани със зародишния център В-клетъчен тип (GCB) на DLBCL, включват маркери за диференциране на зародишния център като CD10 и BCL6, докато гените, свързани с активиран В-клетъчен тип (GCB) клетъчно подобен тип - ABC) DLBCL тип съдържат IRF4 /МАМА1.
Няколко проучвания са установили, че изразът BCL2ген е повече от 4 пъти по-висока с ABC DLBCL, отколкото с DLBCL с GCB. Тези резултати предполагат, че подтиповете GCB и ABC DLBCL са получени от В клетки при различни етапидиференциация. DLBCL с GCB произхожда от зародишния център на В клетките, а DLBCL с ABC произхожда от постзародишния център на В клетките на етапа на плазмена диференциация на лимфоцита.
Генетичният анализ показва, че патогенетичните механизми при ABC и GCB DLBCL са различни. DLBCL с GCB се свързва изключително с t (14, 18) транслокации, включващи BCL2ген и ген на тежката верига на имуноглобулините, както и амплификация на c-rel локуса на хромозома 2р. В допълнение, този лимфом има амплификация на онкогенния mir-17-92 микроРНК клъстер, делеция на туморни супресори PTENи честа аномалия BCL6ген.
Онкогенната амплификация често се отбелязва при ABC DLBCL SPIB, делеция на тумор супресорния локус INK4a/ARFи тризомия 3, което води до изразяване на абнормни КАРТА11, BCL10и A20, които активират IkB кинази и NF-kB пътища на туморна лимфогенеза.
В табл. Фигура 2 показва хистогенетичните и молекулярно-генетичните характеристики на лимфомите при HIV-инфектирани пациенти в зависимост от хистологичния произход на тумора.
Таблица 2.Характеристики на лимфомите, свързани с HIV инфекция
| Хистогенетичен произход | Хистология | Хистогенетични маркери (%) | Молекулярно-генетични маркери (%) | CD4 клетки | ||||
|---|---|---|---|---|---|---|---|---|
| МАМА1 | Син-1 | BCL-2 | BCL-6 | P53 | c-MYC | |||
| Зародишен (зародишен) център | LB | <15 | 0 | 0 | 100 | 60 | 100 | Може да е сравнително запазен номер |
| DLBCL с GCB | <30 | 0 | 0 | >75 | Рядко | 0–50 | Променливо количество | |
| Следзародишен център | DLBCL с ABC | 100 | >50 | 30 | 0 | 0 | 0–20 | Обикновено малки |
| Първичен лимфом на ЦНС | >50 | >60 | 90 | >50 | 0 | 0 | >50 mm 3 | |
| PLE | 100 | >90 | 0 | 0 | 0 | 0 | Променливо количество | |
| плазмобластичен лимфом | 100 | 100 | 0 | 0 | Рядко | 0 | Променливо количество | |
Бележки: KSHV, сарком на Капоши, свързан с херпесен вирус; MUM1 - мултиплен миелом-1.
Диагностика на ХИВ-асоциирани лимфоми
Най-важното диагностично изследване е хистологичното и имунохистохимично изследване на материала, получен от ексцизионна биопсия.
В повечето случаи хистологичната картина на HIV-позитивните лимфоми е подобна на тази, развиваща се при HIV-отрицателни пациенти.
Хистологични характеристики на HIV-асоциираните лимфоми
ХИВ-асоциираният DLBCL се класифицира в 2 хистологични варианта - центробластен и имунобластен. Центробластичният вариант представлява около 25% от HIV-асоциираните лимфоми и се характеризира с дифузен растеж на големи лимфоидни клетки с кръгли или овални ядра и изпъкнали нуклеоли. Те често експресират маркери на зародишния център на фоликулите като CD10 и BCL6 и като цяло всички туморни клетки са CD20 положителни. Имунобластичният вариант на DLBCL съдържа над 90% имунобласти и често показва характеристики на плазмоцитоидна диференциация. Този вариант на DLBCL представлява около 10% от всички HIV-асоциирани лимфоми. Този тумор е CD10 отрицателен, тъй като е лимфом от постфеталния център на фоликула на лимфните възли. Често при DLBCL от имунобластен тип се отбелязва положителна експресия MUM1/IRF4и CD138/синдекан-1 маркери. Този тумор често има митози с висока експресия на Ki-67/MIB-1. При имунобластния лимфом туморните клетки могат да бъдат CD20 отрицателни поради ко-експресия на EBV.
Свързани с активирането маркери като CD30, CD38, CD71 често се експресират в имунобластния вариант на DLBCL.
Туморната клетка при PEL е тумор от В-клетъчен произход, но туморните клетки нямат експресия на В-клетъчни антигени като CD20 и CD79a. CD45, CD30, CD38, CD138 обикновено се експресират и се свързват с KSHV/HHV-8 и EBV.
При плазмобластичен лимфом, като правило, положителна експресия на CD38, CD138 и MUM1/IRF4антигени и отрицателни за CD20 и CD45.
ХИВ-асоциираният BL се разделя на 3 отделни подтипа: класически, плазмоцитоиден, атипичен. Класическият тип BL се диагностицира при приблизително 30% от всички HIV-асоциирани лимфоми и морфологично прилича на класическия BL на HIV-отрицателни пациенти. LP с плазмоцитоидна диференциация се характеризира със среден размер на клетката с изобилна цитоплазма, която много по-често се отбелязва при състояния на тежък имунен дефицит. В други случаи туморните клетки имат силен ядрен плеоморфизъм, с по-малко, но по-видно ядро в миналото даден тип LB беше наречен атипичен LB. И трите типа имат много висок резултат на митотичен индекс с експресия на CD19, CD20, CD79a и CD10 и са отрицателни за BCL2. Случаите на EBV-позитивна LB варират от 30% - с класическа LB, и LB, свързана с плазмоцитоидна диференциация - 50-70%. Класическата HL при HIV-инфектирани пациенти е представена главно от смесен клетъчен вариант, EBV се открива в почти всички случаи на HL. Интересно е, че в ерата на антиретровирусната (ARV) терапия има значително увеличение на честотата на нодуларна склероза на HL поради по-голям дял пациенти с висок брой CD4 клетки.
За диагностицирането на HIV-свързани лимфоми не се използва изследване на генната експресия. Но за да се установи произходът на DLBCL, е необходимо имунохистохимично изследване с използване на CD10, BCL6 и MUM1. Според най-новия диагностичен и прогностичен алгоритъм е необходимо изследване на допълнителни маркери GCET1 и FOXP1. Освен това, според съвременната литература, MYC+ туморните клетки в DLBCL могат да се използват за прогнозиране на резултатите от терапията. Доказа това MYC-позитивните тумори реагират слабо на терапията, използваща режима R-CHOP. Следователно е разумно да се извърши цитогенетично или FISH изследване на тумора за откриване MYCтранслокации, за да се определи най-ефективното лечение.
Клинични характеристики на НХЛ, свързана с ХИВ
ХИВ-свързаните лимфоми се характеризират с бърз растежтумори. Най-често при пациенти от тази категория се открива наличието на В-симптоми (необяснима треска, нощно изпотяване, необяснима загуба на тегло с повече от 10% от нормалното). Увреждането на костния мозък се диагностицира при 25-40% от пациентите, стомашно-чревния тракт - при 26%. Участието на ЦНС в туморния процес при HIV-инфектирани пациенти се регистрира при 12–57% от пациентите.
Комплекс от лабораторни и инструментални изследвания за установяване на разпространението на туморния процес и определяне на прогностичната група при пациенти с ХИВ-асоцииран лимфомдо голяма степен неразличими от тези при HIV-отрицателни пациенти.
Диагностичната и прогностична роля на позитронно-емисионната томография с флуородезоксиглюкоза (PET-FDG) е доказана при пациенти с HIV-отрицателни агресивни лимфоми. Понастоящем ролята на PET-FDG в диагностиката на HIV-свързани лимфоми не е добре разбрана. Предишен опит с PET-FDG при пациенти с HIV-асоциирани лимфоми е ограничен до малък ретроспективен анализ и изисква допълнително проучване. При извършване на PET при пациенти с HIV-асоциирани лимфоми е необходимо също да се проведе диференциална диагноза на туморни лезии, нодуларна реактивна хиперплазия, липодистрофия и инфекция.
Прогностични критерии за ХИВ-асоциирани лимфоми
Международният предсказуем индекс (IPI) е стандартният прогностичен критерий при HIV-отрицателни пациенти с DLBCL. Въпреки това, използването на MPI при пациенти с DLBCL, свързан с HIV, е спорен въпрос. Няколко проучвания показват, че PFS и общата преживяемост не могат да бъдат предвидени, когато MPI се използва при пациенти с HIV-асоциирани лимфоми.
Прогностичната стойност при HIV-инфектирани пациенти е броят на CD4-позитивните лимфоцити. Доказано е, че пациенти с CD4<100 клеток/мкл подвержены повышенному риску развития серьезных оппортунистических инфекций и летального исхода. Кроме того, как отмечалось ранее, у больных с тяжелой иммуносупрессией более часто диагностируют иммунобластный подтип ДВККЛ, большинство из которых являются ABC, они имеют плохие результаты по сравнению с пациентами с сохраненным иммунитетом, где подтип GCB более распространенный . В последнее время опубликованы исследования, в результате которых не установлена связь между происхождением опухолевых клеток и исходом ВИЧ-ассоциированных ДВККЛ .
Засягането на ЦНС, което е повишено при асоциираните с ХИВ агресивни В-клетъчни лимфоми, също носи лоша прогноза.
Лечение на НХЛ, свързана с ХИВ
Лечението на HIV-асоциираните лимфоми може да бъде разделено на 2 етапа: преди използването на АРВ терапия и след широкото използване на специфична комплексна АРВ терапия.
Резултатите от лечението на ХИВ-асоциираните лимфоми преди ерата на АРВ терапията бяха лоши, като средната преживяемост на пациентите беше средно 5-6 месеца и се определяше основно от броя на CD4 клетките. Тези резултати са свързани с развитието както на хематологични, така и на нехематологични усложнения по време на химиотерапия. В едно проучване, L.D. Kaplan et al отбелязват, че високите дози циклофосфамид корелират с ниската преживяемост на пациентите. В опит да се подобрят резултатите от лечението и да се намали рискът от инфекциозни усложнения, беше проведено многоцентрово, рандомизирано проучване, което сравнява резултатите от терапията с mBACOD при стандартни дози и при намаляване на дозата при 192 пациенти с HIV-асоциирани лимфоми.
Както се вижда от табл. 3, броят на пълните отговори, средната преживяемост в групите за сравнение не са статистически различни, но хематологичната токсичност в групата пациенти, използващи ниски дози в режима на mBACOD, е статистически по-ниска. Авторите заключават, че по-ниски дози химиотерапевтични средства са за предпочитане при пациенти с HIV-асоциирани лимфоми. Проучването обаче включва пациенти с малък брой CD4-позитивни лимфоцити. В ерата на широкото използване на АРВ терапията броят на пациентите с голям брой CD4 клетки се е увеличил, което в крайна сметка прави възможно повишаването на ефективността на терапията и намаляването на инфекциозния риск при използване на стандартни дози химиотерапия (вижте Таблица 3 ) .
Таблица 3Резултати от лечението на ХИВ-асоциирани лимфоми според клинични проучвания
| Вид на изследването (брой пациенти, n) | Лимфомен вариант | Терапевтичен режим | Брой CD4 клетки/mm3 | Резултати от терапията | ||||
| Пълна ремисия, % | Оцеляване без прогресия | Обща преживяемост | ||||||
| Kaplan L.D., 1997 | Многоцентрово рандомизирано, фаза III (n=192) | Агресивен НХЛ | m-BACOD + GM-CSF | 107 | 52 | 38 седмици | 31 седмици | |
| m-BACOD ниско + GM-CSF | 100 | 41 | 56 седмици | 35 седмици | ||||
| Ratner l., 2001 | фаза II (n=65) | DLBCL, имунобластен NHL | m-CHOP | 138 | 30 | Среден отговор на терапията - 65 седмици | ||
| ЧОП | 122 | 48 | Не е постигнат среден отговор на терапията | |||||
| Sparano JA, 2004 | фаза II (n=98) | ДВККЛ, ЛБ | диданозин | 90 | 47 | 1-годишен - 42%, 2-годишен - 35% | 6,8 месеца | |
| CDE | 227 | 44 | 1-годишен - 40%, 2-годишен - 38% | 13,7 месеца | ||||
| Муние Н., 2006 | фаза III (n=485) | DVKKL | ХИВ (резултат 0) | ACVBP | 239 | 61 | 5 годишни - 35.54% | 5 годишни - 41.61% |
| ЧОП | 239 | 51 | 5 годишни - 30.49% | 5 годишни - 38.57% | ||||
| ХИВ (резултат 1) | ЧОП | 72 | 49 | 5 годишни - 16.35% | 5 годишни - 18.37% | |||
| CHOP ниско | 72 | 32 | 5 годишни - 10.29% | 5 годишни - 15.34% | ||||
| ХИВ (резултат 2–3) | CHOP ниско | 21 | 20 | 5 годишни - 0,16% | 5 годишни - 2.20% | |||
| СРЕЩУ | 21 | 5 | 5 годишни - 0% | 5 годишни - 0,8% | ||||
| Little R. F., 2003 г. | фаза II (n=39) | DVKCL, LB, PLE | ЕПОХА | 198 | 74 | 4,4 години - 73% | 4,4 години - 60% | |
| Каплан Л.Д., 2005 г | фаза III (n=150) | ДВККЛ, ЛБ | R-CHOP | 130 | 49,5 | 45 седмици | 139 седмици | |
| ЧОП | 147 | 41,2 | 38 седмици | 110 седмици | ||||
| Boue F., 2006 | фаза II (n=61) | DLBCL, LB, имунобластичен, плазмобластен | R-CHOP | 172 | 35 | 2 годишни - 69% | 2 годишни - 75% | |
| Спина М., 2005 | фаза II (n=74) | DLBCL, BL, анапластичен едроклетъчен лимфом, имунобластен | CDE-R | 161 | 70 | 2 годишни - 59% | 2 годишни - 64% | |
| CDE | 227 | 45 | 2 годишни - 38% | 2 годишни - 45% | ||||
| Sparano JA, 2010 | фаза II (n=101) | ДВККЛ, ЛБ | R-DAEPOCH | 181 | 73 | 1-годишен - 78%; 2 годишни - 66% | 2 годишни - 70% | |
| ДАЕПОХ→Р | 194 | 55 | 1-годишен - 66%; 2 годишни - 63% | 2 годишни - 67% | ||||
| Dunleavy K., 2010 | фаза II (n=33) | DVKKL | SC-ЕПОХА-RR | 208 | 5 годишни - 84% | 5 годишни - 68% | ||
Бележки: m-BACOD - метотрексат, блеомицин, доксорубицин, циклофосфамид, винкристин, дексаметазон; GM-CSF колония стимулиращ фактор; CDE - циклофосфамид, доксорубицин, етопозид; R - ритуксимаб; CHOP - циклофосфамид, винкристин, доксорубицин, преднизолон; VS - винкристин, преднизолон; ACVBP - доксорубицин, циклофосфамид, винкристин, блеомицин, преднизолон; EPOCH - етопозид, преднизолон, винкристин, доксорубицин, циклофосфамид; SC - кратък курс; DA е коригираната доза.
Въвеждането на АРВ терапията преди около 15 години оказа значително влияние върху резултата от лечението на ХИВ-асоциираните лимфоми с увеличаване на средната преживяемост, което се обяснява с благоприятния ефект на АРВ терапията върху имунната система. Пациентите с HIV-асоциирани лимфоми, които имат запазена имунна функция, имат по-малък риск от развитие на инфекциозни усложнения, което им позволява да получат оптимално ефективна химиотерапия в пълен обем. Едно проучване показа, че при пациенти с ХИВ-асоцииран лимфом общата преживяемост и преживяемостта без прогресия зависят до голяма степен от АРВ терапията, а не от интензивността на дозите на цитостатичната терапия.
В табл. 3 са представени резултатите от рандомизирани проучвания на различни режими на цитостатична терапия при пациенти с ХИВ-асоциирани лимфоми.
В табл. 4 показва основните схеми за лечение на HIV-асоциирани лимфоми, чиято ефективност е представена в табл. 3.
Таблица 4Основните схеми на цитостатична и поддържаща терапия на HIV-асоциирани лимфоми
| Автор | Тип НХЛ | Име на схемата | Препарати | Доза | Ден на въведението | Предотвратяване на увреждане на ЦНС | Поддържаща грижа |
|---|---|---|---|---|---|---|---|
| Sparano JA, 2010 | DLBCL, PB, PLE, плазмобластен лимфом | R-ЕПОХА-21 | ритуксимаб | 375 mg/m2 | 1-ви ден, повече от 3 часа | Интратекално или цитарабин 50 mg или метотрексат 12 mg седмично в продължение на 4 седмици за 1 цикъл | Филграстим 5 mg/kg на ден 6 след EPOCH Флуконазол 100 mg дневно непрекъснато Ципрофлоксацин 500 mg два пъти дневно 8-15 дни след EPOCH |
| етопозид | 50 mg/m2 | ||||||
| доксорубицин | 10 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| винкристин | 0,4 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| циклофосфамид | 1-ви цикъл: 187 mg/m 2, ако CD4 3 и 375, ако CD4 >100 клетки/m 3 | Ден 5 60 минути инфузия | |||||
| Dunleavy K., 2010 | SC-ЕПОХА-RR-21 | ритуксимаб | 375 mg/m2 | 1-ви и 5-ти ден, повече от 3 часа | Интратекален метотрексат 12 mg на ден 1 и 5 за 3-5 цикъла | Филграстим 5 mg/kg Ден 6-15 след EPOCH Предотвратяване ако CD4<100 кл/м 3 |
|
| етопозид | 50 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| доксорубицин | 10 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| винкристин | 0,4 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| циклофосфамид | 750 mg/m2 | Ден 5 60 минути инфузия | |||||
| Муние Н., 2006 | DVKKL | ACVBP-14 | доксорубицин | 75 mg/m2 | 1-ви ден | Filgrastim 5 mg/kg на 6-ия ден след химиотерапията, докато броят на неутрофилите стане повече от 0,5x10 9 /l Триметоприм/сулфаметоксол 160–800 mg 3 пъти седмично непрекъснато |
|
| циклофосфамид | 1200 mg/m2 | 1-ви ден | |||||
| винкристин | 2 mg/m2 | 1-ви и 5-ти дни | |||||
| блеомицин | 10 мг | 1-ви и 5-ти дни | |||||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| ЧОП-21 | доксорубицин | 50 mg/m2 | 1-ви ден | Интратекален метотрексат 12 mg преди всеки цикъл (максимум 4 инжекции) | |||
| циклофосфамид | 750 mg/m2 | 1-ви ден | |||||
| винкристин | 1,4 mg/m2 | 1-ви ден | |||||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| CHOP ниско-21 | доксорубицин | 25 mg/m2 | 1-ви ден | Интратекален метотрексат 12 mg преди всеки цикъл (максимум 4 инжекции) | |||
| циклофосфамид | 400 mg/m2 | 1-ви ден | |||||
| винкристин | 1,4 mg/m2 | 1-ви ден | |||||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| VS-14 | винкристин | 2 мг | 1-ви ден | Интратекален метотрексат 12 mg преди всеки цикъл (максимум 4 инжекции) | |||
| преднизолон | 60 mg/m2 | 1-ви-5-ти ден | |||||
| Спина М., 2005 | DLBCL, PB, PLE, плазмобластен лимфом | CDE+/-R-28 | ритуксимаб | 375 mg/m2 | 1-ви ден, повече от 3 часа | Интратекален метотрексат 12 mg преди всеки цикъл или цитарабин 50 mg на ден 1 и 4 от цикли 1 и 2 за PD или заболяване на костния мозък | Filgrastim 5 mg/kg на 6-ия ден след химиотерапия Триметоприм/сулфаметоксол 160–800 mg 3 пъти седмично непрекъснато Флуконазол 100 mg дневно непрекъснато |
| циклофосфамид | 185–200 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| доксорубицин | 12,5 mg/m2 | Ден 1-4 (96 часова инфузия) | |||||
| етопозид | 60 mg/m2 | Ден 1-4 (96 часова инфузия) |
Отчитане на риска от инфекции по време и след завършване на химиотерапията, особено при пациенти с брой на CD4<100 клеток/мм 3 , является важным проведение профилактических мер. Все пациенты с ВИЧ-ассоциированной лимфомой, независимо от числа лимфоцитов CD4 на момент установления диагноза и проведения химиотерапии, должны получать профилактику против Pneumocystis jiroveci пневмония, за предпочитане с триметоприм/сулфаметоксазол (1 таблетка 2 пъти дневно 3 пъти седмично по време на лечението и до възстановяване на броя на CD4 >200 клетки/mm3). Пациенти с брой на CD4<50–100 клеток/мм 3 также требуют назначения азитромицина 1200 мг/нед в качестве профилактики развития Mycobacterium avium. Назначаването на валацикловир за предотвратяване на реактивиране на вируса на херпес симплекс е показано само при пациенти, които имат анамнеза за клинични прояви на лабиален и аногенитален херпес. Пациенти с ХИВ-асоцииран лимфом, които са били диагностицирани с хепатит В виремия, се нуждаят от антивирусна терапия. Въпреки това, монотерапията със зидовудин, например, ще увеличи вероятността от специфична HIV мутация, M184V, която може да допринесе за развитието на резистентност към АРВ лекарства и да увеличи хематологичната токсичност на химиотерапията. Пациенти с лигавични инфекции, причинени от Candida, не трябва да приемат азоли едновременно с химиотерапия.
Ролята на АРВ терапията в химиотерапията при пациенти с ХИВ-асоцииран лимфом
Мненията за рисковете и ползите от продължаване на АРВ терапията по време на химиотерапия за агресивни лимфоми са противоречиви. Много изследователи с право са загрижени, че неконтролираната репликация на ХИВ по време на химиотерапия ще доведе до влошаване на имунната функция и че продължаването на АРВ терапията по време на химиотерапията и възстановяването на имунитета може да предотврати развитието на инфекциозни усложнения, особено при пациенти с нисък брой на CD4. Въпреки това, лекарите трябва да бъдат нащрек за потенциални фармакокинетични взаимодействия между АРВ и химиотерапевтични лекарства, особено при АРВ лекарства от първо поколение (зидовудин, ставудин, диданозин, протеазни инхибитори).
Въз основа на резултатите от изследването на взаимодействието на АРВ лекарства от първо поколение и цитотоксични лекарства, редица автори препоръчват спиране на АРВ терапията по време на химиотерапия. Някои изследователи са особено загрижени за техните фармакокинетични и фармакодинамични взаимодействия, които могат да доведат до намаляване на необходимата концентрация на цитостатици, повишаване на токсичността на химиотерапевтичното лечение. W.H. Wilson et al., B.N. В своята работа Phenix показа например, че някои класове антиретровирусни лекарства от първо поколение инхибират апоптозата на лимфоидните клетки и повишават риска от развитие на нови ХИВ мутации.
Понастоящем широко се използват антиретровирусни лекарства от ново поколение, като тенофовир, емтрицитабин, ралтегравир, които се понасят добре, не акумулират странични ефекти от химиотерапевтичното лечение на лимфоми и не повлияват апоптозата на лимфоцитите. В допълнение, в условията на остри опортюнистични инфекции, 4-седмично забавяне на започване на АРВ терапия е свързано със значително повишен риск от развитие на СПИН или смърт. Пациентите с ХИВ-асоцииран лимфом обикновено имат съпътстващи опортюнистични инфекции и средно 7-седмично забавяне на ARV терапията по време на химиотерапия може да има отрицателни последици като цяло. Все пак трябва да се помни, че пациентите с ХИВ-асоцииран лимфом изискват 4-6 цикъла химиотерапия, което може да увеличи продължителността на прекъсването на АРВ терапията и да повлияе негативно на преживяемостта на пациентите като цяло. М.Х. Батеганя и В.О. Mwanda, в резултат на тяхното изследване, доказа ясно предимство за оцеляване на пациенти с ХИВ-асоцииран лимфом, като същевременно предписва АРВ терапия и химиотерапия.
Клиничен случай
Пациент А., на 43 години, се оплаква от обща слабост, болки в корема, киселини, загуба на тегло с 20 kg през годината.
Антителата срещу ХИВ бяха открити за първи път на 7 септември 2012 г., когато пациентът беше изследван за клинични и епидемиологични показания (загуба на тегло, активен хроничен хепатит С, история на инжекционна употреба на наркотици).
От анамнезата: болен през последната година; през юли 2011 г. е диагностицирана стомашна язва; многократно провеждана противоязвена терапия амбулаторно и стационарно, без подобрение. 4 пъти извършена фиброгастродуоденоскопия (FGDS) с биопсия. Едно проучване (февруари 2012 г.) разкрива езофагеална кандидоза. Въпреки това, бдителността за ХИВ инфекцията, ранната диагностика на рак на стомаха не е отбелязана.
На преглед FGDSот 31.08.2012 г.: в антрума по всички стени има туморовидно образувание, деформиращо стомаха, ригидно, контактно кървене, на места с фибринова обвивка. Тези промени се отнасят до пилора и луковицата на дванадесетопръстника. Пилорът като такъв не е дефиниран, представляващ грудкова формация.
Резултати от хистопатологично изследване № 4327-40 от 06.09.12 г.: материалът съдържа фрагменти от гнойно-възпалителна гранулационна тъкан и некротичен детрит. Картината ни позволява надеждно да преценим само наличието на язвен процес. Препоръчителен контрол след противоязвена терапия, при възможност - повторна биопсия за получаване на интактна тъкан.
На 13 септември 2012 г. пациентът се обърна към отделението по СПИН на клиниката на Института по епидемиология и инфекциозни болести на името на V.I. Л.В. Громашевски.
При допълнително изследване: CD4 - 8,7%, което е 147 клетки/µl; ХИВ вирусен товар - 1325 РНК копия/мл.
Взето е решение за повторно изследване на хистологичните препарати, получени чрез биопсия от 31.08.2012 г. в специализирана лаборатория.
Резултатът от хистологично и имунохистохимично изследване № 12CSD6049 от 02.10.2012 г.: в препаратите се определя гладка мускулна тъкан (мускулна тъкан на стомаха) с плътна инфилтрация от големи лимфоцитни клетки с малък брой малки лимфоцити. Ядрото на туморните клетки е везикуларно, съдържа 2-3 базофилни ядра. Има много фигури на митоза и апоптоза в тумора. Морфологичната картина е най-съответстваща на едроклетъчния лимфом. Според имунохистохимичен анализ, туморните клетки са положителни за CD20, отрицателни за CD3, CD30 и общи цитокератини. Също така туморните клетки са положителни за CD10, отрицателни за bcl6, MUM-1, което показва техния произход от зародишния център. Заключение: DLBCL на стомаха, центробластичен вариант, с фенотип на клетки от герминативния (зародишен) център.
По-нататъшното лечение и наблюдение на пациента се извършва съвместно с хематолог. Води се разследване.
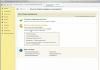
Според направените PET/CT: се отбелязват метаболитно активни и структурни промени в долната трета на стомаха, не се установяват костно-деструктивни промени (Фиг. 1).

Ориз. един.Резултатите от PET/CT при диагностицирането на стомашен лимфом при пациент A.
Данните за анализ на биохимията и периферната кръв са представени в таблица. 5, 6.
Таблица 5Резултатите от анализа на периферната кръв на пациент А.
Таблица 6Резултатите от биохимичен кръвен тест на пациент А.
Извършено е генотипизиране за носителство на алела HLA-B*5701.
Въз основа на резултатите от изследването се поставя диагнозата:
HIV инфекция. IV клиничен стадий. ХИВ-свързан неходжкинов стомашен DLBCL IIE от зародишния център, T2N0M0. Кандидоза на устната лигавица, хранопровода. Хроничен вирусен хепатит С, репликативна форма, HCV+ РНК, генотип 3а, 1.2×106 копия.
Преди започване на химиотерапия на пациента е предписана АРВ терапия: ABC/3TC+LPV/rit (комбинация абакавир/ламивудин + комбинация лопинавир/ритонавир)
Проведен 1 курс на полихимиотерапия R-CHOP-21 и два курса на CHOP-21 в стандартни дози на фона на симптоматична терапия. Ритуксимаб е прекратен, тъй като броят на CD4 е намалял до 90 клетки/mcL след прилагане на ритуксимаб и се е развила тежка неутропения.
След всеки курс на химиотерапия на 7-ия ден филграстим се прилага в доза от 5 mg/kg, докато абсолютният брой на неутрофилите се увеличи с 1x10 9 /l или повече. За профилактика Pneumocystis jiroveci пневмонияпредписан триметоприм/сулфаметоксол 960 mg 3 пъти седмично непрекъснато. За да се предотвратят бактериални инфекции, пациентът приема моксифлоксацин 400 mg веднъж дневно в продължение на 10 дни след всеки курс на химиотерапия. Като се има предвид развитието на кандидозен стоматит по време на химиотерапия, на пациента е предписан флуконазол 200-400 mg дневно непрекъснато, средно 10 дни.
След завършване на 3-тия курс на химиотерапия, пациентът е диагностициран с пълна ремисия, което се потвърждава от резултатите от PET-CT изследване на 20 декември 2012 г. (след 3 курса на химиотерапия). В сравнение с предишния PET-CT от 11 октомври 2012 г. се отбелязва намаляване на дебелината на стените на стомаха до 0,75 cm по малката и по-голямата кривина. В долната трета на стомаха дебелината на стената намалява до 0,85 см. Не се открива повишаване на метаболитната активност. Заключение: В-клетъчен лимфом на стомаха, състояние след 3 курса полихимиотерапия. PET-CT картина на пълна метаболитна регресия и частично морфологична (фиг. 2).
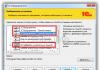
Въпреки това пациентът след приключване на химиотерапията развива оригване на развалени яйца, повръщане на несмляна храна, спастична болка в епигастралната област. Според рентгеновото изследване на стомаха (21.12.2012 г.) се установява декомпенсирана стеноза на изхода на стомаха. По време на FGDS (08.01.2013 г.) хранопроводът е проходим, лигавицата е бледорозова, едематозна, множество линейни несливащи се ерозии с размер до 10 mm. Стомахът не се разширява добре с въздух, на празен стомах количеството мътна секреторна течност, слуз и жлъчка се увеличава значително. Перисталтиката е запазена. Гънките са запазени, еластични. Сърдечна гънка II степен. Дифузна еритема на лигавицата в стомаха. В антрума има ярко петниста еритема и мозаечен модел на лигавицата. Гънките са грапави, удебелени, усукани, с неравна повърхност. Пилорът е стенотичен, невъзможно е да се премине апарат с диаметър 9 мм в дванадесетопръстника. Заключение: рефлуксен езофагит, стеноза на изхода на стомаха (фиг. 3).

Ориз. 3.Рентгенова снимка на стомаха на пациент А.
Като се има предвид цикатричната деформация на долната трета на стомаха с декомпенсирана стеноза на пилора, храносмилателна кахексия и асцит, беше взето решение за целесъобразността на хирургическата палиативна интервенция. След адекватна предоперативна подготовка (корекция на водно-протеин-електролитния метаболизъм, установяване на хранителна назоинтестинална сонда) се извършва операция в размер на байпасна предна напречна дебелочревна гастроентероанастомоза с браунова фистула (според Velfer-Shalimov), дренаж на коремна кухина. Следоперативният период е относително задоволителен, без усложнения. От 10-ия ден се наблюдава положителна динамика в евакуацията на стомашното съдържимо на фона на адекватна поддържаща терапия, което направи възможно добавянето на перорални фракционни хранителни добавки за кърмачета към парентералното и ентералното хранене. Назогастралната декомпресионна сонда заедно с прекъснати кожни конци бяха отстранени на 14-ия ден от постоперативния период. Пациентът е изписан от болницата на 15-ия ден.
По този начин, докато се постави диагнозата ХИВ, много пациенти могат да развият лимфом. За да се изключи диагностична грешка, хистологичният материал трябва да се изпраща за изследване само в специализирана хистопатологична лаборатория. Характеристиките на клиничната картина и лечението на HIV-асоциираните лимфоми, както и високият риск от развитие както на инфекциозни, така и на неинфекциозни усложнения по време на химиотерапия, изискват по-нататъшно проучване за подобряване на прогнозата на заболяването като цяло. Въпреки че агресивната полихимиотерапия е възможна при много пациенти с имунна недостатъчност, тя е придружена от тежки странични ефекти и изисква добре координирано взаимодействие между хематолог-онколог и специалист по лечение на HIV инфекция, често включвайки специалисти от различен профил в процеса на лечение. .
Списък на използваната литература
1. Диагностична онкохематология (2011) / Ed. Д.Ф. Глузман. Киев: DIA, 256 с.
2. Alizadeh A.A, Eisen M.B., Davis R.E. et al. (2000) Различни видове дифузен голям В-клетъчен лимфом, идентифициран чрез профилиране на генната експресия. Природа, 403 (6769): 503–511.
3. Амбиндер Р.Ф. (2001) Лимфопролиферации, свързани с вируса на Epstein-Barr, при СПИН. Евро. J. Cancer, 37 (10): 1209–16.
4. Bateganya M.H., Stanaway J., Brentlinger P.E. et al. (2011) Предиктори за оцеляване след диагностициране на неходжкинов лимфом в среда с ограничени ресурси: ретроспективно проучване на въздействието на ХИВ инфекцията и нейното лечение. J. на Синдроми на придобита имунна недостатъчност, 56 (4): 312–319.
5. Besson C., Goubar A., Gabarre J. et al. (2001) Промени в свързания със СПИН лимфом след ерата на силно активната антиретровирусна терапия. Кръв, 98 (8): 2339–44.
6. Biggar R.J., Jaffe E.S., Goedert J.J. et al. (2006) Лимфом на Ходжкин и имунна недостатъчност при хора с ХИВ/СПИН. Кръв, 108 (12): 3786–91.
7. Boue F., Gabarre J., Gisselbrecht C. et al. (2006) Фаза II проучване на CHOP плюс ритуксимаб при пациенти с ХИВ-асоцииран неходжкинов лимфом. J.Clin. Oncol., 24 (25): 4123–28.
8. Boulanger E., Gerard L., Gabarre J. et al. (2005) Прогностични фактори и резултат от първичен ефузионен лимфом, свързан с човешки херпесвирус 8 при пациенти със СПИН. J.Clin. Oncol., 23 (19): 4372–80.
9. Carbone A. (2003) Възникващи пътища в развитието на свързани със СПИН лимфоми. Lancet Oncol., 4 (1): 22–29.
10. Carbone A., Gloghini A. (2005) Свързани със СПИН лимфоми: от патогенеза до патология. бр. J. Haematol., 130 (5): 662–670.
11. Castillo J.J., Winer E.S., Stachurski D. et al. (2010) Клинични и патологични разлики между пациенти с плазмобластен лимфом, положителни за човешки имунодефицитен вирус и отрицателни за човешки имунодефицитен вирус. Левк. Лимфом, 51 (11): 2047–53.
12. Чадбърн А., Чиу А., Лий Дж.Й. et al. (2009) Имунофенотипен анализ на свързан със СПИН дифузен голям В-клетъчен лимфом и клинични последици при пациенти от клинични изпитвания на консорциума за злокачествени заболявания на СПИН 010 и 034. J. Clin. Oncol., 27 (30): 5039–48.
13. Choi W.W., Weisenburger D.D., Greiner T.C. et al. (2009) Нов алгоритъм за имунооцветяване класифицира дифузния голям В-клетъчен лимфом в молекулярни подтипове с висока точност. Clin. рак. Res., 15 (17): 5494–02.
14. Colomo L., Loong F., Rives S. et al. (2004) Дифузните големи В-клетъчни лимфоми с плазмобластна диференциация представляват хетерогенна група от болестни единици. Am. J. Surg. Pathol., 28 (6): 736-747.
15. Dalla-Favera R., Migliazza A., Chang C.C. et al. (1999) Молекулярна патогенеза на В-клетъчно злокачествено заболяване: ролята на BCL-6. Curr. Горна част. микробиол. Immunol., 246: 257–263.
16 . Дейв С.С., Фу К., Райт Г.В. et al. (2006) Молекулярна диагностика на лимфома на Бъркит. Н. англ. J. Med., 354 (23): 2431–42.
17. Davis R.E., Brown K.D., Siebenlist U. et al. (2001) Активността на конститутивния ядрен фактор kappaB е необходима за оцеляването на активирани В-клетъчно-подобни дифузни големи В-клетъчни лимфомни клетки. J. Exp. Med., 194 (12): 1861–74.
18. Davis R.E., Ngo V.N., Lenz G. et al. (2010) Хронична активна В-клетъчна рецепторна сигнализация при дифузен голям В-клетъчен лимфом. Природа, 463 (7277): 88–92.
19. Dunleavy K., Little R.F., Pittaluga S. et al. (2010) Ролята на туморната хистогенеза, FDG-PET и кратък курс на EPOCH с ритуксимаб с плътна доза (SC-EPOCH-RR) при ХИВ-асоцииран дифузен голям В-клетъчен лимфом. Кръв., 115 (15): 3017–24.
20. Dunleavy K., Wilson W.H. (2010) Роля на молекулярния подтип при прогнозиране на изхода от свързан със СПИН дифузен голям В-клетъчен лимфом. J.Clin. Oncol., 8 (16): e260–e262.
21. Dunleavy K., Mikhaeel G., Sehn L.H. et al. (2010) Стойността на позитронно-емисионната томография в прогнозата и оценката на отговора при неходжкинов лимфом. Левк. Лимфом., 51 допълнение 1: 28–33.
22. Fan W., Bubman D., Chadburn A. et al. (2005) Различни подгрупи на първичен ефузионен лимфом могат да бъдат идентифицирани въз основа на техния профил на клетъчна генна експресия и вирусна асоциация. J. Virol., 79 (2): 1244–51.
23. Gaidano G., Capello D., Carbone A. (2000) Молекулярната основа на лимфомагенезата, свързана със синдрома на придобита имунна недостатъчност. Семин. Oncol., 27 (4): 431–441.
24. Gaidano G., Capello D., Cilia A.M. et al. (1999) Генетичната характеристика на HHV-8/KSHV-позитивен първичен ефузионен лимфом разкрива чести мутации на BCL6: последици за патогенезата на заболяването и хистогенезата. Гени Хромозоми Рак., 24 (1): 16–23.
25. Gaidano G., Carbone A., Pastore C. et al. (1997) Честа мутация на 5' некодиращата област на гена BCL-6 при неходжкинови лимфоми, свързани със синдром на придобита имунна недостатъчност. Кръв., 89 (10): 3755-62.
26. Hans C.P., Weisenburger D.D., Greiner T.C. et al. (2004) Потвърждение на молекулярната класификация на дифузен голям В-клетъчен лимфом чрез имунохистохимия с помощта на тъканен микрочип. Кръв, 103 (1): 275–282.
27. Hummel M., Bentink S., Berger H. et al. (2006) Биологично определение на лимфома на Бъркит от транскрипционно и генетично профилиране. Н. англ. J. Med., 354 (23): 2419–30.
28. Kaplan L.D., Lee J.Y., Ambinder R.F. et al. (2005) Ритуксимаб не подобрява клиничния резултат в рандомизирано проучване фаза 3 на CHOP със или без ритуксимаб при пациенти с ХИВ-асоцииран неходжкинов лимфом: Консорциум за СПИН-злокачествени заболявания Проучване 010. Blood, 106(5): 1538–43.
29. Kaplan L.D., Straus D.J., Testa M.A. et al. (1997) Ниска доза в сравнение със стандартна доза m-BACOD химиотерапия за неходжкинов лимфом, свързан с инфекция с вируса на човешката имунна недостатъчност: Национален институт по алергии и инфекциозни болести СПИН Група за клинични изпитвания. Н. англ. J. Med., 336 (23): 1641–48.
30. Klein U., Gloghini A., Gaidano G. et al. (2003) Анализът на профила на генна експресия на свързан със СПИН първичен ефузионен лимфом (PEL) предполага плазмобластична деривация и идентифицира PEL-специфични транскрипти. Кръв, 101 (10): 4115–21.
31. Landgren O., Goedert J.J., Rabkin C.S. et al. (2010) Циркулиращи свободни от серум леки вериги като предсказващи маркери за свързан със СПИН лимфом. J.Clin. Oncol., 28 (5): 773–779.
32. Little R.F., Wilson W.H. (2003) Актуализация на патогенезата, диагностиката и терапията на свързания със СПИН лимфом. Curr .Infect. дис. Rep., 5 (2): 176–184.
33. Lenz G., Staudt L.M. (2010) Агресивни лимфоми. Н. англ. J. Med., 362 (15): 1417–29.
34. Ленц Г., Райт Г.В., Емре Н.К. et al. (2008) Молекулярни подтипове на дифузен голям В-клетъчен лимфом възникват по различни генетични пътища. Proc. Natl. акад. наука САЩ, 105 (36): 13520–25.
35. Ленц Г., Дейвис Р.Е., Нго В.Н. et al. (2008) Онкогенни CARD11 мутации в човешки дифузен голям В-клетъчен лимфом. Наука, 319 (5870): 1676–79.
36. Little R.F., Pittaluga S., Grant N. et al.(2003) Високоефективно лечение на лимфом, свързан със синдром на придобита имунна недостатъчност, с коригирана доза EPOCH: въздействие на спирането на антиретровирусната терапия и биологията на тумора. Кръв, 101 (12): 4653–59.
37. Mounier N., Spina M., Gabarre J. et al. (2006) Неходжкинов лимфом, свързан със СПИН: окончателен анализ на 485 пациенти, лекувани с адаптирана към риска интензивна химиотерапия. Кръв, 107 (10): 3832–40.
38. Mwanda W. O., Orem J., Fu P. et al. (2009) Дозо-модифицирана орална химиотерапия при лечението на свързан със СПИН неходжкинов лимфом в Източна Африка. J.Clin. Oncol., 27 (21): 3480–88;.
39. Ngo V.N., Davis R.E., Lamy L. et al. (2006) Екран за РНК интерференция със загуба на функция за молекулярни цели при рак. Природа, 441 (7089): 106–110.
40. Парех С., Поло Дж.М., Шакнович Р. и др. (2007) BCL6 програмира клетките на лимфома за оцеляване и диференциация чрез различни биохимични механизми. Кръв, 110 (6): 2067–74.
41. Phenix B.N., Cooper C., Owen C. et al. (2002) Модулиране на апоптоза от HIV протеазни инхибитори. Апоптоза, 7 (4): 295–312.
42. Phenix B.N., Lum J.J., Nie Z. et al. (2001) Антиапоптотичен механизъм на HIV протеазни инхибитори: предотвратяване на загуба на митохондриален трансмембранен потенциал. Кръв, 98 (4): 1078–85.
43. Rabkin C.S., Yang Q., Goedert J.J. et al. (1999) Генни варианти на хемокин и хемокинов рецептор и риск от неходжкинов лимфом при индивиди, инфектирани с човешки имунодефицитен вирус-1. Кръв, 93: 1838.
44. Ratner L., Lee J., Tang S. et al. (2001) Химиотерапия за неходжкинов лимфом, свързан с вируса на човешката имунна недостатъчност, в комбинация с високоактивна антиретровирусна терапия. J.Clin. Oncol., 19 (8): 2171–78.
45. Ribera J.M., Oriol A., Morgades M. et al. (2008) Безопасност и ефикасност на циклофосфамид, адриамицин, винкристин, преднизон и ритуксимаб при пациенти с дифузен голям В-клетъчен лимфом, свързан с човешкия имунодефицитен вирус: резултати от проучване фаза II. бр. J. Haematol., 140 (4): 411-419.
46. Роте М., Сарма В., Диксит В.М. et al. (1995) TRAF2-медиирано активиране на NF-kappa B от TNF рецептор 2 и CD40. Наука., 269 (5229): 1424–27.
47. Спарано Дж.А., Лий Дж.Й., Каплан Л.Д. et al. (2010) Rituximab плюс паралелна инфузионна EPOCH химиотерапия е много ефективна при HIV-свързан В-клетъчен неходжкинов лимфом. Кръв, 115 (15): 3008–16.
48. Sparano JA, Lee S., Chen M.G. и др. (2004) Изпитване фаза II на инфузионен циклофосфамид, доксорубицин и етопозид при пациенти с ХИВ-асоцииран неходжкинов лимфом: проучване на Източна кооперативна онкологична група (E1494). J.Clin. Oncol., 22 (8): 1491-1500.
49. Spina M., Jaeger U., Sparano J.A. et al. (2005) Ритуксимаб плюс инфузионен циклофосфамид, доксорубицин и етопозид при ХИВ-асоцииран неходжкинов лимфом: обобщени резултати от 3 проучвания фаза 2. Кръв, 105 (5): 1891–97.
50. Swerdlow S.H., Campo E., Harris N.L. et al. (2008) Класификация на СЗО на тумори на хематопоетични и лимфоидни тъкани. Лион, Франция: IARC.
51. Thompson L.D., Fisher S.I., Chu W.S. et al. (2004) ХИВ-асоцииран лимфом на Ходжкин: клинико-патологично и имунофенотипно изследване на 45 случая. Am. J.Clin. Pathol., 121 (5): 727-738.
52. Tulpule A., Sherrod A., Dharmapala D. et al. (2002) Експресия на множествена лекарствена резистентност (MDR-1) при лимфоми, свързани със СПИН. Левк. Res., 26 (2): 121-127.
53 . Vega F., Chang C.C., Medeiros L.J. et al. (2005) Плазмабластните лимфоми и плазмобластните миеломи на плазмените клетки имат почти идентични имунофенотипни профили. мод. Pathol., 18 (6): 806–815.
54. Zolopa A.R., Andersen J., Komarow L. et al. (2009) Ранната антиретровирусна терапия намалява прогресията/смъртта на СПИН при индивиди с остри опортюнистични инфекции: многоцентрово рандомизирано стратегическо проучване. ПЛОС. Едно, 4 (5): e5575.
55. DeVitaV.T., Lawrence T.S., Rosenberg S.A. (2012) Рак: Принципи и практика на онкологията, 9e
VIL-асоцииран неходжкинов лимфом
О.А. Карнабеда 1, Л.И. Гетман 2 , С.М. Антоняк 2 , Т.В. Рослякова 3 , О.В. Шулига-Недайхлибова 3
1 Национален медицински университет на името на О.О. Богомолец
2 Институт по епидемиология и инфекциозни болести на името на Л.В. Громашевски
3 Медицинска клиника "Иновация"
Резюме.Статията представя характеристиките на клиничната картина, диагностиката и лечението на асоциираните с VIL неходжкинови лимфоми. По-голямата част от лимфомите, свързани с VIL, са в съответствие с класификацията на СЗО от 2008 г. за дифузни B-едроклетъчни лимфоми. За свързаните с VIL лимфоми е характерен типичен растеж на подуване, често при тези пациенти се показва наличието на B-симптоми. Лезиите на кистозния малък мозък се диагностицират при 25-40% от пациентите, а тези на чревния тракт - при 26%. Радиацията в процеса на подуване на ЦНС при HIV-инфектирани пациенти се регистрира при 12–57% от пациентите. Пациентите с VIL-асоциирани лимфоми, при които имунната функция е запазена, могат да имат по-нисък риск от развитие на инфекциозни състояния, което им позволява да разпознаят оптимално ефективната химиотерапия в общото състояние.
Ключови думи:ВІL-асоцииран лимфом, лечение, диагностика.
ХИВ-асоцииран неходжкинов лимфом
О.А. Карнабеда 1 , Л.И. Гетман 2, С.Н. Антоняк 2, Т.В. Рослякова 3 , О.В. Шулига-Недайхлибова 3
1 Национален медицински университет на името на O.O. Богомолец
2 Институт по епидемиология и инфекциозни болести на името на L.V. Громашевски
3 Онкологичен център "ИННОВАЦИЯ".
резюме.В тази статия клиничните характеристики, диагностиката и лечението на ХИВ-асоцииран неходжкинов лимфом. Повечето HIV-асоциирани лимфоидни тумори, според класификацията на СЗО, 2008 г., са дифузни едроклетъчни лимфоми. За HIV-на асоциираните лимфоми се характеризира с бърз растеж на тумора и най-честата при тези пациенти се определя от наличието на B-симптоми. Костният мозък се диагностицира при 25-40% от пациентите, стомашно-чревният тракт - при 26%. По време на процеса на привличане в ЦНС туморът при HIV-инфектирани се определя при 12–57% от пациентите. Пациентите с ХИВ-асоциирани лимфоми, чиято имунна функция е запазена, имат по-малък риск от инфекция, така че можете да им предпишете оптимално ефективна химиотерапия в пълен размер.
ключови думи:ХИВ-асоцииран лимфом, лечение, диагностика.
Церебралният лимфом е рядко, но изключително опасно заболяване. Възрастните хора и тези с отслабена имунна система са склонни към появата му. За съжаление, към днешна дата този вид лекарства не са изобретени за онкологията и пациентите могат да разчитат само на забавяне на неизбежната смърт.
Причини за възникване на лимфома
Причините за развитието на лимфома условно се разделят на две категории. Това е влиянието на външни фактори и вътрешни процеси в тялото. Околната среда играе важна роля в развитието на онкологията на мозъка.
Животът или работата в зона с висока радиация в 97% от случаите провокира развитието на рак. Предпоставка за появата на заболяването е и влиянието на такива токсични вещества като винилхлорид, газ, който се използва в много индустрии, аспаркам, използван като заместител на захарта.
Има версия, че електромагнитното излъчване от мобилни телефони и електропроводи може да доведе до лимфом. Въпреки че тази теория не е получила научно потвърждение.
Вътрешните фактори, които стават тласък за развитието на лимфома, са:
- подложени на лъчева терапия за лечение на някакво заболяване;
- отслабен имунитет в резултат на HIV инфекция;
- имунна недостатъчност след предотвратяване на отхвърляне на имплантирани донорски органи.
Генетичната предразположеност играе важна роля в развитието на рак на мозъка. Медицината познава случаи, когато лимфомът засяга роднини от първи ред. При такива пациенти в юношеството се появяват множество тумори с доброкачествен характер, но без подходящо лечение те могат да се трансформират в ракови клетки. От родителите, диагностицирани с ХИВ, повече от 10% от децата се раждат с мозъчен лимфом.
Също така, онкологията може да се появи на фона на мононуклеоза, вирусна болест на Epstein-Barr и хромозомни мутации. Напоследък лекарите отбелязват увеличение на броя на пациентите с рак на мозъка. Причината за това е влошаването на общата екологична обстановка в големите градове и хранителните навици на съвременния човек. Все по-често голям брой храни, съдържащи канцерогени, започнаха да се консумират в храната.
Видове мозъчни лимфоми
Ракът на мозъка се класифицира в няколко вида. Така е по-лесно да се направи обща картина на заболяването и да се избере правилното лечение.
- Ретикулосаркома. Произхожда от клетки на ретикулума. На практика това е изключително рядко, така че не беше възможно да се разбере историята на произхода му до края. Болестта лесно се бърка с лимфосаркома. Симптоматологията на ретикулосаркома е множествена и зависи от мястото на локализацията и етапа на развитие. Първоначално се появява в лимфните възли. Болестта е чувствителна към лъчева терапия. При ранна диагностика и лечение пациентът има приблизително 10 години ремисия.
- Микроглиома. Най-опасният вид лимфом, тъй като мястото на локализацията му не винаги позволява пълно лечение. Злокачествените ракови клетки растат много бързо и са почти нелечими. Доброкачествените неоплазми се разпространяват по-бавно, може да не се проявяват доста дълго време. Микроглиома се диагностицира при половината от пациентите с мозъчни тумори. Заболяването се появява от глиални тъкани на клетъчно ниво. Това е първичен тип образувания, които не проникват в костната черепна тъкан и във вътрешната обвивка на мозъка. Има вид на плътен съсирек от розов или червеникаво-сив цвят без ясни граници. Може да нарасне до 15 см в диаметър. Болестта може да засегне всеки, включително деца.
- Дифузен хистиоцитен лимфом. В процеса на протичане на заболяването настъпва разрушаването както на отделните мозъчни клетки, така и на неговите тъкани. Метастазите се разпространяват доста бързо, имат дифузен характер и, когато покълнат в здрави тъкани, дават нови импулси на централната нервна система. Пациентът се чувства горещ, изпотява се обилно и бързо губи тегло. Но въпреки факта, че този вид онкология има агресивна форма, тя е доста лечима.
В зависимост от мястото на проявление на лимфома се разделя единична или множествена изолирана лезия на мозъчната тъкан. В 10% от случаите се засягат очите със засягане на мозъчните обвивки, с разпространение към гръбначния мозък.
Симптоми на проява на лимфом
При мозъчен лимфом симптомите нямат специфични прояви, което значително усложнява диагностиката на заболяването. Онкологията може да се подозира по следните признаци:
- повишено вътречерепно налягане, което причинява постоянно главоболие, което не изчезва след приемане на болкоуспокояващи, увеличава се сутрин, в легнало положение, при навеждане. Може да бъде придружено от гадене или повръщане;
- изключване на определени функции на частта от мозъка, която туморът притиска. Това може да бъде парализа на лицевия нерв, загуба на говор, намалено зрение, пълна или частична загуба на усещане от която и да е страна на тялото и др.;
- психични разстройства. Болният човек губи концентрация, става разсеян, практически не отговаря на въпроси. Усещането за сънливост се увеличава, което може да прерасне в летаргия. В някои случаи човек може да стане груб, шегите стават плоски, чувството за самокритика изчезва, апетитът се увеличава до ненаситност;
- епилептични припадъци. Периодично има конвулсии със загуба на съзнание или потрепване на всяка мускулна група. Тези симптоми се срещат със следната честота: неврологичен дефицит в 70% от случаите, психични разстройства в 43%, признаци на интракраниална хипертония в 33%, конвулсии в 14%. При пациенти с ХИВ епилептичните припадъци се срещат в 25% от случаите, а енцефалопатията често се развива на възраст 30-40 години.
В по-късните стадии на лимфома настъпват промени в личността. Човек става емоционално нестабилен, реакциите му са непредвидими, появяват се пропуски в паметта.
Диагностика на мозъчен лимфом
Диагностицирането на рак на мозъка не е лесно. Обикновено кръвният тест не показва наличието на патологични промени в тялото и симптомите са неинформативни. Ако подозирате наличието на лимфом, лекарят трябва да извърши пълен преглед на пациента. Като начало се провеждат серия от неврологични тестове, за да се идентифицират нарушенията на рефлексната функция, координацията на движенията, функционирането на мускулите и сетивните органи. Пълна диагноза е възможна само при пълна клинична картина, но в този случай практически няма шанс за хирургично лечение. За ранна диагностика на мозъчен лимфом се използват редица инструментални и лабораторни методивключително следните дейности:
- магнитно-резонансна терапия, която се извършва чрез въвеждане на контрастно вещество през вената в тялото. Мозъчен лимфом на ЯМР се вижда на компютъра поради натрупването около образуването на това вещество. който се натрупва около неоплазмата;
- томографията ще покаже наличието на тумор в тялото;
- трепанобиопсия - изследване на биоматериал, взет от мозъчна тъкан след отваряне на черепа;
- стереотактична биопсия. Това е биопсичен анализ, който се получава чрез вземане на мозъчна тъкан през дупка, направена в черепа;
- електроенцефалограма. Използва се за откриване на фокуса на нарушенията на мозъчния биопотенциал, тяхната критичност и влияние върху дейността на централната нервна система като цяло;
- рентгеновото изследване ви позволява да прецените наличието на вторични признаци на лимфом и хипертония в мозъка;
- за изследване на бебета се използва ултразвуковият метод.
 Томографията е един от методите за диагностика на мозъчния лимфом
Томографията е един от методите за диагностика на мозъчния лимфом В допълнение към всичко по-горе, на пациента се предписва кръвен тест и биохимия. За определяне на първичния лимфом на мозъка се извършват рентгенови лъчи, за вторичния - ултразвук.
Начини за лечение на рак на мозъка
След като се диагностицира мозъчен лимфом, лечението се предписва въз основа на етапа на развитие на заболяването, местоположението на тумора и неговия размер. Не винаги е възможно да се избере правилната терапия поради кръвно-мозъчната бариера, която забавя навлизането на лекарствата в тялото и неутрализира някои от техните компоненти. Общо има три начина за спиране на развитието на метастази поне временно: химиотерапия, лъчева терапия и операция.
Химиотерапия
Церебралният лимфом се повлиява добре от лечение с химиотерапия. В зависимост от вида на тумора и неговата чувствителност към различна група лекарства може да се предпише моно- или полихимиотерапия. Лекарствата се прилагат на пациента чрез спинална пункция, т.к. Именно този подход дава максимална ефективност на лекарствата.
Изборът на определени лекарства се определя само от лекуващия лекар. Обикновено метотрексатът се предписва за курс на монохимиотерапия. Ако е необходимо да се използва комбинация от средства, тогава се предпочитат цитарабин, темозоломид или етопозид.
Въпреки факта, че химиотерапията има добри предпоставки за постигане на ремисия, тя не е лишена от негативни последици. Това се дължи на факта, че лекарствата действат не само върху болните клетки, но и върху здравите. Проява странични ефектизависи от избраното лекарство и неговата дозировка. Това може да бъде силно гадене и замаяност, загуба на коса, сухота в устата, загуба на тегло, неизправност на стомашно-чревния тракт и намаляване на защитните функции на тялото. Ако химиотерапията е дала положителни резултати и няма място за вторична инфекция, тогава пациентът може да очаква ремисия след няколко години.
Лъчетерапия
Лечението чрез облъчване е доказан и ефективен метод, но не винаги в случай на мозъчен лимфом. Ако се използва, тогава само в комбинация с "химия" или операция за трансплантация на костен мозък. Това решение е особено важно за пациенти с ХИВ анамнеза.
Хирургическа интервенция
Операциите за отстраняване на тумор в главата практически не се извършват, т.к. това може да доведе до нарушаване на умствената и нервната дейност. Всякакви опити за радикална намеса водят до наранявания на мозъчните структури на дълбоко ниво.
 Хирургията е едно от леченията за мозъчен лимфом.
Хирургията е едно от леченията за мозъчен лимфом. Единственият вид операция, която е възможна в случай на рак на мозъка, е трансплантация на стволови клетки. Но тази процедура се извършва само за пациенти в млада възраст и не гарантира положителен резултат.
Прогноза за лимфома
При мозъчен лимфом прогнозата за оцеляване не е обнадеждаваща. Според статистиката само 75% от пациентите получават ремисия до 5 години, но при условие, че терапията е била проведена навреме. В напреднала възраст цифрата намалява до 40%. Възможните рецидиви увеличават смъртността сред пациентите почти два пъти. Добри показатели могат да се получат, ако се проведе радикална терапия и не се остави туморът да расте в кратък период от време. В такива случаи продължителността на живота може да бъде удължена до 10 години.
Източник: www.oonkologii.ru
Обща концепция за лимфоми на централната нервна система
Неоплазмата е по-често вторична лезия в стадий 4 на различни видове неходжкинови лимфоми. Това означава, че първоначално се отбелязва растеж в лимфните възли, след което настъпва разпространение с образуването на екстранодални (екстранодални) огнища.
Първичният лимфом на централната нервна система (PCNS) е тумор, произхождащ от лимфоидната тъкан, който произхожда от главния или гръбначния мозък и не излиза извън тях. За поставяне на такава диагноза е необходим обстоен преглед и пълна увереност в липсата на лезия извън нервната система.

Сред първичните локализации PLCNS се нарежда на второ място след стомашните лимфоми. Той е доста рядък (в структурата на първичните мозъчни тумори неговият дял е не повече от 5%). Глобалните данни за заболеваемостта са 5-5,5 на 1 милион население.
Въпреки това през последните десетилетия се наблюдава значително увеличение на неходжкиновите лимфоми, включително PLCNS. Ето защо, когато се провежда диференциална диагноза на образувания на централната нервна система, които заемат пространство, винаги трябва да се има предвид този тип злокачествени образувания.
Интересът към този тумор се дължи и на факта, че той е изключително чувствителен към химиотерапия и в 50% от случаите е възможно да се постигне пълна ремисия.
Морфологично PLCNS е представен в 90% от дифузен едроклетъчен В-клетъчен лимфом. Това е силно злокачествена форма.
Рискови групи
Основният от тях е пациентите с имунна недостатъчност. PLCNS се диагностицира при 6-10% от ХИВ-позитивните лица. Средно това усложнение настъпва 5 години след първоначалната диагноза на HIV инфекцията. В почти 100% от случаите появата на лимфом при тези пациенти е свързана с вируса на Epstein-Barr. Средната възраст на пациентите е 30-40 години, 90% от тях са мъже.
Втората група, при която PLCNS се среща много по-често от останалите (според някои източници 150 пъти), са тези, които получават имуносупресивна терапия във връзка с трансплантация на органи. Средната възраст на пациентите е 55 години.
Увеличение на заболеваемостта се наблюдава и при хора без имунен дефицит. В тази група обаче средната възраст е по-висока - над 60 години. Мъжете също боледуват по-често (3:2 срещу жени). Причините за растежа не са надеждно ясни, лекарите се придържат към вирусната теория.
Класификация на лимфомите на ЦНС
Няма поетапно градиране на PLCNS. Наличието на едно или повече огнища, както и увреждането на различни части на централната нервна система, не оказва влияние върху прогнозата на заболяването и избора на метод на лечение.
Лимфомите се класифицират според анатомичната локализация: единична или множествена изолирана лезия на мозъчната тъкан, огнища в мозъка със засягане на окото (в 10% от случаите), със засягане на менингите, с разпространение в гръбначния мозък, изолирана лезия на гръбначния мозък, изолирана лезия на окото. В 85% от случаите първичният церебрален лимфом се намира супратенториално, т.е. в полукълбата, а в 15% - инфратенториално (малък мозък, вентрикуларна област, мозъчен ствол). В полукълбата по-често се засягат фронталните дялове (20%).
Как изглежда лимфомът на ЦНС?
По локализация туморът може да се прояви като единични огнища, различни по размер, разположени в полукълба, в базалните ганглии и в corpus callosum. В 35% от случаите има много огнища (по-често при хора с имунен дефицит). Лезиите на гръбначния мозък могат да възникнат първоначално (70% в лумбалната област) или да се разпространят от мозъка през продълговатия мозък чрез директна инфилтрация (цервикална и гръдна), както и разпространение на туморни клетки в цереброспиналната течност.
Микроскопски лимфомът е периваскуларно (около съдовете) натрупване на имунобласти или центробласти с инфилтрация на мозъчната тъкан.
Симптоми
мозък
При този тумор няма специфичен симптомокомплекс. Клинично е възможно да се подозира обемно образуване на мозъка на следните основания:
1. Повишено вътречерепно налягане. Проявява се като избухващо главоболие, което не се облекчава от конвенционалните болкоуспокояващи, засилва се сутрин, в легнало положение, при навеждане, придружено от гадене или повръщане.
2. Неврологичен дефицит. Това е загуба на определени функции поради спирането на частта от мозъка, която туморът притиска.
- Нарушаване на движението на крайниците (с увреждане на левия фронтален лоб - вдясно, с дясната локализация - вляво). Движенията или напълно липсват (парализа), или са силно ограничени (пареза).
- Афазията е нарушение на речта.
- Двойно виждане или загуба на зрителни полета, рязко намаляване на зрението.
- Нарушения на преглъщането (задушаване).
- Промяна в чувствителността на дясната или лявата половина на тялото.
- Парализа на лицевия нерв.
- Загуба на слуха.
- Замайване, нестабилност при ходене с увреждане на малкия мозък.
3. Психически отклонения. Вниманието и концентрацията значително се влошават, пациентите са потиснати, трудно е да се отговори на въпроси. Може да се развие сънливост до летаргия. Признаци на челната психика: пациентите са небрежни, критиката намалява, склонност към плоски шеги, груби, ненаситни, сексуално обезсърчени.
4. Припадъци. Генерализирани конвулсии със загуба на съзнание или периодично потрепване на всяка мускулна група. Тези симптоми на церебрален лимфом се срещат със следната честота: неврологичен дефицит в 70% от случаите, психични разстройства в 43%, признаци на интракраниална хипертония в 33%, конвулсии в 14%. При хората с HIV инфекция епилептичните припадъци са по-чести (при 25%), като чест признак при тях е и развитието на енцефалопатия в млада възраст (30-40 години).
Гръбначен мозък
Поражението на този отдел на централната нервна система се проявява чрез признаци на компресия: нарушено движение, чувствителност, загуба на рефлекси, уринарна и фекална инконтиненция.
Диагностика
Основен
Откриването на лимфома не е лесно. Въпреки че е условно и се отнася до хематологични заболявания, обикновено няма промени в кръвния тест. Ако се открият горните симптоми, неврологът предписва:
- Преглед от офталмолог.
- Електроенцефалография.
- CT или MRI на главния или гръбначния мозък с и без контраст.
Лимфомът има определени признаци, които позволяват да се подозира още на етапа на невроизображение. На ЯМР - единични или множествени фокуси, които са или с по-ниска плътност, или не се различават от околната мозъчна тъкан, обикновено хомогенни, понякога пръстеновидни. С въвеждането на контраста те го натрупват интензивно. Перифокален оток, калцификации, кръвоизливи и изместване на медианните структури са по-рядко срещани, отколкото при други първични тумори на ЦНС.
Диагнозата трябва да бъде потвърдена хистологично. Стереотактичната биопсия (STB) е стандартът за съмнение за първичен мозъчен лимфом. Не се препоръчва предписването на стероиди преди процедурата, тъй като поради техния цитолитичен ефект те могат значително да променят размера и хистологичната структура на тумора. Отворена биопсия се извършва само в случаите, когато STP не може да се извърши (например, ако е локализиран в мозъчния ствол). При спинален лимфом се извършва ламинектомия за вземане на биопсия.

Полученият материал се изследва хистологично, както и имунохистохимична идентификация (определяне на CD45 антигена).
Изясняваща диагностика
При потвърдена диагноза лимфом, пациентът се изследва допълнително за:
- Търсене на екстраневрален лимфомен фокус.
- Изключване или потвърждение на имунодефицит (HIV).
- Общи оценки на състоянието за определяне на прогнозата и предстоящото лечение.
Назначен:
- Разширен кръвен тест.
- Биохимичен анализ с определяне на лактат дехидрогеназа (LDH), креатининов клирънс, албумин, урея, трансаминази.
- Спинална пункция с общо клинично и цитологично изследване на цереброспиналната течност.
- Определяне на антитела срещу HIV.
- Тест за антитела срещу вируса на Епщайн-Бар, херпес, токсоплазмоза, сифилис, вирусен хепатит.
- CT сканиране на гръдния кош.
- Ултразвук на лимфни възли.
- ЯМР на корем, малък таз.
- Фиброгастроскопия.
- Пункция на костния мозък.
- При мъжете ултразвук на тестисите.
- При необходимост ПЕТ, спирометрия, ехокардиография Общото състояние на онкоболния се оценява по скалата на Карновски (0-100%) или ECOG (0-4 точки).
Лечение
Хирургичното лечение на първичните лимфоми на ЦНС обикновено не се прилага. Изключение е значителното компресиране на мозъчните структури или гръбначния мозък.
Основният метод за лечение на такива тумори е системната химиотерапия и последващото облъчване на останалите огнища.
Най-ефективното лекарство за PLCNS е метотрексат. Прилага се самостоятелно или в комбинация с други цитостатици, по-често с цитарабин. Клиничните проучвания с rituximab също показват добри резултати.
За пълен терапевтичен ефект са необходими достатъчно високи дози метотрексат (до 10 g / m2). Но това лекарство е много токсично, причинява потискане на хемопоезата, дисфункция на бъбреците и черния дроб и невропатия. Затова е важно да се избере режим, който пациентът може да понесе - лечебни дози с висока токсичност или палиативни дози с ниска токсичност.
Метотрексат се прилага чрез интравенозна инфузия само в болнични условия. За да се намали токсичността, е необходимо допълнително да се използва калциев фолинат (левковорин) и да се инжектират големи обеми течност. Курсът е от 4 до 8 цикъла на всеки 2 седмици.
След завършване на курса на химиотерапия се извършва лъчетерапия на мозъка, включително очите. Общата доза обикновено е 30-36 Gy, режимът е 2 Gy на сеанс 5 пъти седмично. Ако след химиотерапия, според MRI, туморните огнища продължават, тогава се предписва допълнително локално облъчване.
При пациенти с първичен спинален лимфом RT се счита за основен метод след хирургично отстраняване на компресията на гръбначния мозък. Въпреки това, поради много рядката поява на тази локализация на PLCNS, данните все още са недостатъчни.
Прогноза
Продължителността на живота на пациент с PLCNS без терапия е не повече от 2 месеца. Навременната диагностика и започнатият адекватен комплексен ефект позволяват пълно излекуване на 70% от пациентите. Прогнозата за мозъчен лимфом е индивидуална и зависи от много фактори. За PLCNS има специален международен прогностичен индекс IELGS. Въз основа на него, като се вземат предвид рисковите фактори на пациента, е възможно да се прогнозира общата 2-годишна преживяемост.
Рискови фактори
- Възраст над 60 години.
- Състоянието на пациента по скалата ECOG е повече от 2 точки (индекс на Карновски> 50%).
- Повишен плазмен LDH.
- Повишаване на концентрацията на протеин в цереброспиналната течност.
- Увреждане на дълбоките структури на мозъка.
Прогнозата за 2-годишна преживяемост при наличие на 1 фактор е 80%, 2-3 - 48%, а дефинирането на 4-5 фактора намалява тази цифра до 15%.
Основни изводи
Първичният лимфом на ЦНС е рядък тумор. Но има свои собствени характеристики, които го отличават от другите злокачествени тумори на нервната система.
Основни характеристики на PLCNS:
Среща се по-често при хора с отслабен имунитет.
Ако се подозира лимфом, не трябва да се прилагат стероиди, докато не бъде направена биопсия.
За разлика от други мозъчни тумори, той не може да се оперира.
Отговаря добре на химиолъчева терапия.
Източник: RosOnco.ru
Причините
Има два вида фактори, които провокират развитието на патологията:
- Външно негативно влияние;
- Вътрешни процеси, водещи до развитие на лимфом.
Лекарите препоръчват да се обръща повече внимание на влиянието на факторите на околната среда върху мозъка. Когато човек живее на места с високи нива на радиация, в 97 от 100% се откриват проблеми в главата с онкологичен характер. Основата за развитието на рак е вещество - газ. Винилхлорид се използва във фабрики, които произвеждат аспаркаме и заместител на захарта за диабетици.
Има твърдения, че развитието на злокачествен тумор в главата идва от електромагнитно излъчване, както и от вредното въздействие на телефони или електропроводи с високо напрежение. Вярно е, че науката все още не е успяла да потвърди истинността на предположенията.
Когато причината външен видустановено, трябва внимателно да обмислите какво е в състояние да провокира развитието на тумор в мозъка отвътре:
- Облъчване по време на лъчева терапия.
- При HIV заболяване защитните функции на тялото са значително намалени. Той не е в състояние да се бори с развиващата се патология.
- След операция по трансплантация на органи. В тази ситуация пациентът развива имунодефицит.
Лекарите не изключват наследствеността да е една от причините за появата на дегенерирали мозъчни клетки. Ако роднините по първа линия са станали източник на болестта, тогава детето все още има младостнаблюдавана клинична картина. Въпреки това, на първия етап неоплазмите са доброкачествени. Когато няма лечение, рискът от преход на клетките от здрави към ракови се увеличава.
Мононуклеозата също причинява развитие на онкологичен тумор вътре в черепа. Допълнителни причини:
- вирусна болест на Epstein-Barr;
- Мутации в двойки хромозоми.
Всеки ден се регистрира, че броят на пациентите с фатално заболяване расте. Скок на заболяванията често се регистрира в големите столични райони. Трябва да обърнете внимание и на храната. В големите търговски обекти и на пазара по-рядко се среща продукт, отгледан естествено и узрял благодарение на слънцето, а не канцерогенен състав.
Симптоми
Опасността от заболяването се крие в липсата специални функциинеразположения. Диагнозата е трудна, тъй като пациентът не се оплаква от влошаване.
За да се определят възможните проблеми в тялото, лекарите препоръчват да се обърне внимание на всеки симптом, описан по-долу.
Повишено вътречерепно налягане
Провокират се интензивни главоболия. Синдромът не изчезва дори след приемане на болкоуспокояващи. На сутринта главоболието става по-интензивно. В легнало положение и при навеждане болката се засилва. Често допълнителни симптоми са повръщане и гадене.
Загуба на функция
Пациентът губи определени функции, контролирани от частта на органа на главата, където се намира неоплазмата. В резултат на това увеличаването на размера на тумора води до натиск върху зоните, пациентът губи умения.
Разстройства на психичното здраве
Пациентът не може да се концентрира, често е разсеян и не може да отговори на прости въпроси. Пациентът е склонен да спи, способен да се превърне в летаргия.

В други случаи човек е активен, но когато говори, може да бъде груб. Опитва се да се шегува, но това са плоски, безсмислени шеги. Пациентът престава да се самокритикува. Има апетит, достигащ до лакомия.
епилептични припадъци
Пациентът отбелязва появата на конвулсивни явления, припадък, не е изключено потрепване на пръст или ръка.
Честотата на проява на симптомите от тази група: 70% - неврологичен дефицит, 43% - психични разстройства, 33% - вътречерепно налягане, 14% - конвулсивни явления. от HIV инфекцияимунитетът на пациента намалява и след това се наблюдават епилептични пристъпи при 25% от пациентите. Енцефалопатията засяга повече от 50% от пациентите на възраст от 30 до 40 години.
Последните етапи на лимфома водят до промяна на личността на пациента. Има нестабилност в настроението, емоциите. Невъзможно е да се предвидят действията и реакциите на човек. Пациентът развива проблеми с паметта, когато няма периоди на спомени.
Класификация
Онкологията на органа на главата е разделена на три вида. За да се проведе лечението с резултат, е необходимо ясно да се определи степента на увреждане. човешкото тялои източник на анормални клетки.
Помислете за видовете мозъчни увреждания.
Ретикулосаркома
Клетките на съединителната тъкан на хемопоетичните органи по определени причини стават злокачествени. Лекарите рядко се сблъскват с това заболяване. Следователно патологията остава неизследвана докрай. Клиничната картина на заболяването е подобна на лимфосаркома. Това винаги са множество огнища на развитие на патология, в зависимост от местоположението и степента на развитие на заболяването.
микроглиома
Лимфом, приписван на опасни видовепатология. Туморът се намира там, където е невъзможно да се извърши пълна терапия. Болните клетки растат бързо, обемът на засегнатата тъкан се увеличава. Не реагира на лечение. Ако доброкачественият тумор е проникнал в мозъка, тогава растежът на патологията е бавен, без външни прояви.
Микроглиома се открива при 50% от пациентите с неоплазма в мозъка. Глиалните тъкани служат като основа за растеж. Туморът не расте и не засяга слоевете на органа, не расте в костната тъкан. На екрана се вижда плътен съсирек с размити ръбове. Регистрирани са случаи, когато размерът на тумора достига 15 сантиметра. Микроглиомът се развива при възрастни и деца.
Дифузен хистиоцитен лимфом
Болестта разрушава мозъка отвътре. Първо, отделните клетки са обект на унищожаване, след това тъканите страдат. Развитието и разпространението на тумора е бързо. Метастазите се разпространяват в тялото, засягайки здравите тъкани. Централна нервна системаполучава нови импулси от вече увредени тъкани. Телесната температура на пациента се повишава, потенето се увеличава, телесното тегло намалява. Този вид онкологично заболяване, бързо разпространяващо се в тялото, е чувствително към продължаващо лечение.
Лимфомът на централната нервна система и GM е способен да образува единен фокус на развитие на патология и множество огнища. При 10 от 100 болни от този вид рак са засегнати очите, обвивките на органа в черепа, засегнат е и гръбначният мозък.
В по-голямата част от случаите на лимфом неоплазмата се разпространява в мозъчните полукълба (85%). Засягане на малкия мозък може да възникне в 15% от случаите. Същият брой пациенти имат тумор във вентрикулите на мозъка и в багажника.
Диагностика
Вече беше казано, че диагнозата на заболяването се извършва само в случай на посещение при лекар поради друго заболяване. Кръвният тест не се счита за надежден източник за определяне на тумор, така че е необходим цялостен преглед, предписан от лекар.
За процедурата се използва следното медицинско оборудване:
- ЯМР. Пациентът първо се инжектира с контрастно вещество. На ЯМР веднага ще се появи лимфом, опростен от всички страни с контрастен агент.
- Томография. Тук изследването ще потвърди наличието на тумор и ще предупреди за необходимостта от лечение.
- Трепанобиопсия. Това е изследване на част от биологичния материал, взет от мястото на лезията след отваряне на черепа.
- Стереотактична биопсия. Тук полученият биоматериал идва през дупка в костите на черепа.
- Електроенцефалограма. Този метод може да се използва, когато източникът на патологията е изяснен. Измерва се влиянието и критичността на ситуацията с централната нервна система.
- Рентгенов. Снимката показва вторичен признак на онкология и вътречерепно налягане.
- Изследването при деца се извършва с ултразвук.
Лечение
Лекарят, след като получи данни от изследвания, потвърждаващи диагнозата лимфом, предписва лечение на индивидуална основа. Три начина за борба:
- Терапия с химикали;
- излагане на радиация;
- Операция.
Химиотерапия
Ефективен начин за борба с рака. Онкологът индивидуално избира лекарства, изчислява дозата. Използването на няколко лекарства едновременно дава по-голям резултат.

Често има комбинация от химиотерапия и лъчетерапия. Препарати, съдържащи химикали:
- цитарабин;
- етопозид;
- Метотрексат;
- циклофосфамид;
- Хлорамбуцил и др.
За лечение се използват лекарства с моноклонални антитела. Недостатъкът на използването на химикали за лечение е, че унищожава болните и здравите клетки едновременно.
Странични ефекти след курс на химиотерапия:
- Развива се анемия, водеща до слабост в тялото и мускулите.
- Повръщане, гадене.
- Разстройство на храносмилателната система.
- Косопад.
- Постоянно усещане за сухота. В същото време в устната кухина се появяват малки рани и рани по лигавицата.
- Телесното тегло бързо намалява.
- Защитната обвивка на тялото не работи. Това означава, че инфекциите от трети страни свободно влизат в тялото.
Ако трябва да направите анестезия, вземете Celebrex.
Излагане на радиация
Тъй като химиотерапията не винаги дава положителни резултати при лечението на онкологията, излагането на радиация се превръща в допълнително средство, което засилва ефекта на първото. Излагането на радиация достига метастази, унищожавайки източника на екскреция. Не се използва като независим начинборба с онкологията.
Лимфомът на мозъка се нарича рядко заболяванезасягащи лимфоидната тъкан. Заболяването има злокачествен характер и е концентрирано предимно в мозъчните обвивки. Опасността от патология е, че тя се проявява в последните етапи, което утежнява лечението. Ситуацията се усложнява от факта, че кръвно-мозъчната бариера не позволява използването на методи за лечение на заболяването, които успешно се справят с лимфоми в други части на тялото.
Правете разлика между неходжкинов лимфом и болест на Ходжкин. В първия случай туморът се развива в случай на мутация на една лимфоцитна клетка. При засягане на цялата лимфна система започва болестта на Ходжкин.
Неходжкиновите лимфоми на мозъка са първични или вторични. Най-често мъжете са засегнати от това заболяване. Първичният тумор рядко се появява в мозъка. По-често се образува поради метастази и е вторичен.

В В-клетките има следните видове тумори:
- Дифузен едроклетъчен лимфом. Диагностицира се в 30% от случаите, главно сред възрастните хора. Лечимо е лесно и повечето пациенти живеят повече от 5 години след откриване на заболяването.
- Дребноклетъчен лимфоцитен лимфом. Туморът расте бавно, но е силно злокачествен. Този вид лимфом се среща при 7% от пациентите. Този тумор може да се изроди в тумор с бърз растеж.
- Фоликуларен лимфом. Доста често срещан тумор, диагностициран в 22% от случаите. Расте бавно и има ниска злокачественост. В риск са хората над 60 години. Болестта се лекува лесно, 60% от пациентите живеят повече от 5 години.
- Лимфом от клетките на зоната на мантията. Такъв тумор расте бавно, но прогнозата за лечението му е неблагоприятна, тъй като само 20% от пациентите оцеляват. Такъв лимфом се среща в 6% от случаите.
- Лимфом на Бъркит. Болестта се диагностицира при хора над 30 години, предимно сред мъжете. Среща се много рядко, само в 2% от случаите. Успехът на лечението зависи от етапа, на който е открита патологията. Навременната химиотерапия увеличава шансовете за възстановяване.

Т-туморите се класифицират, както следва:
- Т-лимфобластен злокачествен лимфом. Засяга млади хора на 20 години. Той е диагностициран в 75% от случаите. Шансовете за оцеляване се увеличават, ако заболяването се диагностицира навреме. Ако туморът е засегнал гръбначния мозък, възстановяването е малко вероятно и се наблюдава само при 20% от пациентите.
- Анапластичен едроклетъчен лимфом. Патологията се среща при млади хора. Възстановяването е възможно, ако лечението започне навреме.
- Екстранодален Т-клетъчен лимфом. Патологиите, податливи на хора от всяка възраст, могат да се появят в различни възрастирезултатът зависи от стадия на заболяването.

Ретикулосаркома
Ретикулосаркомът е злокачествена пролиферация на клетки от ретикуларната лимфоидна тъкан. Тя не се появява дълго време. Само в по-късните етапи, когато се появят метастази, черният дроб и далакът на пациента се увеличават и може да започне жълтеница.
Първичният ретикулосарком се локализира в лимфните възли. На този етап лимфните възли са много плътни и не болят. С течение на времето туморът прораства в близките тъкани, в резултат на което се нарушава кръвообращението и лимфния поток. Когато се разпространява в лимфните възли на медиастинума, неоплазмата притиска хранопровода и трахеята. Метастазите в коремната кухина водят до прекомерно натрупване на течност в долната част на корема и ако съдовете, преминаващи в гръдната кухина, са повредени, възниква синдром на компресия. Растежът в червата води до неговото запушване.
микроглиома
Отнася се за първични злокачествени лимфоми. Неоплазмата се състои от атипични микроглиални клетки.
Дифузен хистиоцитен лимфом
Злокачествена форма на заболяването, характеризираща се с големи клеткилимфоми с обилна цитоплазма и полиморфни ядра. такива клетки са способни на фагоцитоза, абсорбирайки главно еритроцитите. Много рядко се диагностицира.
Лимфом на костния мозък
Костният мозък съхранява стволовите клетки на еритроцитите, тромбоцитите и левкоцитите. Повишеното делене на лимфоцитите води до изместване на кръвните клетки. По този начин се нарушава хемопоезата. Тази патология се нарича лимфом на костния мозък. Дълго време не показва никакви признаци и се открива само на етапи 3-4.

Болестта е трудна за лечение, ефективността на терапията се влияе от вътрешни и външни фактори.
Причините
Точните причини за мозъчния лимфом са неизвестни. В хода на медицинските изследвания е установено, че мозъчният лимфом се развива при отслабена имунна система. Патологиите благоприятстват:
- HIV инфекция;
- излагане на радиация;
- генетично предразположение;
- системно влияние на канцерогени, които включват тежки метали и различни химикали;
- вирус на Epstein-Barr;
- Инфекциозна мононуклеоза;
- условия на околната среда;
- трансплантация на органи;
- кръвопреливане;
- възраст след 60 години.
Описаните фактори при определени условия провокират развитието на болестта, особено с комплексен ефект.

Външни фактори
Има външни фактори, които могат да причинят мозъчен лимфом. Между тях:
- излагане на радиация;
- газ винилхлорид, който се използва в производството на пластмаси;
- аспартамът е заместител на захарта.
Причините за развитието на болестта не са точно установени. Повечето лекари смятат, че електромагнитните полета и далекопроводите с високо напрежение допринасят за появата на лимфома.
Слаба имунна система
Хората с нарушена работа са изложени на риск от развитие на първичен церебрален лимфом имунна система. Причините за лимфома при имунодефицит са:
- Трансплантация на органи.
- наследствено предразположение.
- Контакт с канцероген.
Ако здрав човек развие лимфом, той обикновено се развива в лимфните възли. При пациенти с вируса на имунната недостатъчност заболяването прогресира в гръбначния или главния мозък.
генетично предразположение
Причината за развитието на рак е генетична предразположеност. Членовете на едно и също семейство са изправени пред появата на доброкачествени тумори, но ако лечението се пренебрегне, те могат да се превърнат в рак. Децата с ХИВ често се раждат с мозъчен лимфом.
Неврофиброматозните заболявания причиняват развитието на тумори на гръбначния мозък. Заболяването се наследява от роднини от първи ред.

Симптоми
Хората с лимфом в мозъка изпитват следните симптоми в различна степен:
- нарушение на речта;
- водянка;
- зрително увреждане;
- увреждане на нервите без възпаление;
- изтръпване на ръцете;
- халюцинации;
- психични разстройства;
- нарушена координация на движенията;
- висока температура;
- главоболие;
- световъртеж;
- драстична загуба на тегло.

Симптоматологията на лимфома се изостря от факта, че патологията може да доведе до исхемичен инсулт и кръвоизлив. Възникналите хематоми нарушават мозъчната дейност и провокират развитието на енцефалопатия.
Диагностика
За точната диагноза на лимфома се използват редица лабораторни методи. Между тях:
- компютърна томография.
- Спинална пункция за изследване на цереброспиналната течност.
- Рентгеново изследване на гръдния кош за изследване на състоянието на лимфната система.
- Трепанобиопсия - изследване на мозъчна тъкан за наличие на лимфом чрез отваряне на черепа.
- Магнитен резонанс на мозъка.
- Стереотактична биопсия за хистологично изследване.
- Общ кръвен анализ.
Ако няма достатъчно информация за изследване на материала, е възможно да се използва ултразвуково изследване или биопсия на костен мозък, което може да открие заболяването в ранен стадий на развитие.

Терапия
Възможно ли е да се излекува мозъчен лимфом с химиотерапия, няма консенсус сред лекарите. В повечето случаи се практикува комплексно лечение на мозъчен лимфом. По време на химиотерапията състоянието на пациента се подобрява, ако при лечението се използват големи дози лекарства. Лекарствата се избират индивидуално, като се вземе предвид чувствителността на лимфома към определени вещества. Препоръчително е да се използва химиотерапия заедно с курс на лъчева терапия, което увеличава продължителността на живота на пациента. Това важи особено за пациентите, заразени с ХИВ.
За да се премахнат симптомите на заболяването, се използват наркотични лекарства, които могат да намалят болката. Операцията не се препоръчва, тъй като съществува риск от неврологично увреждане поради случайно увреждане на тъканите около лимфома. Операцията е трудна и поради трудността да се установят ясни граници на тумора.
Десенсибилизацията започва с група нестероидни противовъзпалителни средства (ненаркотични аналгетици), като кетани, найз или аертал. Това са слаби болкоуспокояващи и ефектът може да не е достатъчен дори в началния етап. От лекарствата, които могат да се продават в аптека без рецепта, по-добре е да поискате Celebrex. За закупуване на наркотични вещества ще ви е необходим формуляр за рецепта 107-1 / y-NP. Розовият формуляр се получава от терапевта.

Заболяването в пренебрегвана форма се лекува с помощта на палиативна медицина, чиято същност е да осигури емоционална подкрепа на пациента и да подобри цялостното благосъстояние. Главоболието на този етап е толкова силно, че не може да се премахне с наркотични аналгетици.

Прогноза
При липса на лечение животът на пациента е няколко месеца. Химиотерапията може да увеличи преживяемостта до две години. След курс на лъчетерапия пациентите с ХИВ и СПИН могат да живеят около 10 месеца.
Злокачествените лезии се намаляват с помощта на трансплантация на стволови клетки. Първичният мозъчен лимфом е труден за лечение. Младите хора имат по-добра прогноза за оцеляване от възрастните хора. Трябва да се помни, че при лечението на химиотерапия са възможни странични ефекти. Те включват ниски нива на белите кръвни клетки, тъканна смърт и нарушено съзнание.
Облъчването също води до негативни последици. Пациентите имат предимно неврологични заболявания, понякога години след процедурата.

Лимфомът е патологично злокачествено новообразувание, състоящо се от активно размножаващи се атипични лимфоцити, които образуват тумор. Такава формация засяга лимфоидната тъкан, може да се появи в различни органи. Първичният церебрален лимфом е доста рядко заболяване, диагностицирано при пет души на милион население. Сред всички първични образувания на мозъка, 1-3% от всички случаи се падат на дяловете на лимфома.
Класификация
Има неходжкинов лимфом и болест на Ходжкин. Първият вариант се характеризира с появата на тумор поради мутация на една лимфоцитна клетка и може да засегне мозъка. Лимфомът на Ходжкин засяга цялата лимфна система, кръстен на учения, който първи описва патологията.
Неходжкиновите образувания могат да бъдат първични и вторични, като по-често засягат мъжете. Първичните неоплазми в мозъка са изключително редки, по-често туморът възниква поради метастази от различно местоположение и се нарича вторичен.
Според класификацията на СЗО се разграничават следните видове В-тумори:

Т-туморите включват:

медиастинални лимфоми
Ракът на медиастинума се среща главно при възрастни на възраст 20-40 години. Честотата на поява е 3-7% от всички видове неоплазми с различна локализация и злокачественост. В по-голямата си част в медиастинума не се среща рак, а доброкачествени тумори, в съотношение 80 към 20. Що се отнася до лимфомите, те се образуват в лимфната система на медиастинума.  Основните признаци, за които трябва да внимавате, са увеличаването на лимфата
Основните признаци, за които трябва да внимавате, са увеличаването на лимфата
възли на шията или аксиларните синуси. В началото те могат да бъдат безболезнени, по-късно се появява дискомфорт, болка и зачервяване в засегнатата област на медиастинума. Също така, ракът на медиастинума има такава характеристика като дихателни усложнения, появата на дисфагия или недостиг на въздух. Може да се появи хриптене или кашлица. Всичко това се дължи на растежа на лимфома в медиастиналната кухина и облекчаването на нормалното функциониране на дихателната система.
По правило няма смисъл да се използва хирургически метод, тъй като атипичните клетки се пренасят с лимфния поток до различни органи, това е особена трудност при лечението на лимфоми. Както и в случая с мозъка, основният метод остава курс на лъчева и химиотерапия. Често образуването на лимфом в медиастинума става причина за вторична поява на тумор в мозъка в резултат на метастази.
Да се допълнителни методивключва трансплантация на костен мозък, методът е иновативен, но скъп и специфичен. Както и имунотерапия за подобряване на цялостната устойчивост на организма, потиснато заболяване и курс на химиотерапия.
причини
Ракът няма точна причина. Но в същото време злокачественият лимфом се образува по-често на фона на отслабен имунитет към основните фактори възможна появавключват:
- наличието на HIV инфекция;
- излагане на излагане на радиация;
- генетично предразположение;
- систематично взаимодействие с канцерогени, особено с химикали и тежки метали;
- Инфекциозна мононуклеоза;
- трансплантация на органи и кръвопреливане;
- възраст след 60 години.
Лимфомът на Бъркит в повечето случаи се развива в резултат на инфекция с вируса на Епщайн-Бар и това е доказан факт. Освен този случай, останалата част от списъка е само възможни фактори, които могат да увеличат риска от провокиране на заболяването при определени условия, но не се считат за доказани причини.
Клинична картина
Лимфомът има симптоми, обикновено се проявява чрез притискане на мозъчната тъкан. Те включват: 
- главоболие и световъртеж;
- зрителни, слухови и обонятелни халюцинации;
- психични разстройства;
- нарушена координация или загуба на усещане в определена част от тялото;
- конвулсии и внезапни епилептични припадъци;
- слухови и зрителни смущения;
- подуване на регионалните лимфни възли;
- внезапни кръвоизливи;
- повръщане.
Заедно с тези признаци, когато ракът не е в начален стадий, се появяват общи симптоми, характерни за онкологията на всяка локализация:
- загуба на апетит;
- слабост;
- увреждане;
- внезапна загуба на тегло;
- покачване на температурата;
- висока температура.
В някои случаи няма такива прояви, така че трябва да сте внимателни към тялото си. Фокални признаци се наблюдават при 73% от пациентите, личностни и психични промени при почти 50% от пациентите. Една трета от пациентите изпитват повръщане и главоболие. Епилептичните припадъци се срещат при 15% от пациентите, а зрителните нарушения - само при няколко процента. Някои пациенти отбелязват липсата на симптоми в ранен стадий на рак или лекото им проявление. В случай, че злокачественият лимфом се развива вторично, на фона на метастази от друг орган, могат да бъдат присъщи специфични признаци на първичния тумор. В някои случаи метастазите се откриват по-бързо от основната неоплазма. Понякога в ранните стадии ракът не показва никакви признаци.
Диагностични мерки
 Неходжкиновият лимфом се идентифицира най-добре чрез ядрено-магнитен резонанс. За по-голяма информативност на метода, пациентът се инжектира с контрастен агент, който открива раковите клетки и се натрупва в тях, което ви позволява да получите по-подробна картина на случващото се.
Неходжкиновият лимфом се идентифицира най-добре чрез ядрено-магнитен резонанс. За по-голяма информативност на метода, пациентът се инжектира с контрастен агент, който открива раковите клетки и се натрупва в тях, което ви позволява да получите по-подробна картина на случващото се.
Ако се подозира рак, независимо от локализацията, биопсията е задължителен метод за изследване, който позволява получаване на увредени тъкани за хистологично изследване. Допълнителният анализ определя вида и структурата на тумора, както и степента на неговото злокачествено заболяване. Освен вземане на тъканни проби от самия тумор, се прави и пункция от клетки на гръбначния мозък.
Извършва се рентгенова снимка на гръдния кош, за да се види състоянието на лимфната система на медиастинума и тимусната жлеза.
В допълнение към инструменталните изследвания, системно се изискват лабораторни кръвни тестове за проследяване на реакцията на тялото към неоплазмата.
Терапия
Неходжкиновият лимфом на мозъка е труден за лечение, тъй като органът има кръвно-мозъчна бариера, която го предпазва от увреждане. Поради това повечето методи просто не са в състояние радикално да повлияят на неоплазмата.
Лимфомът на Бъркит и другите му разновидности са по-добри  обикновено са лечими с курс на химиотерапия. Може да се предпише курс на моно- или полихимиотерапия. В зависимост от вида на лимфома и неговата чувствителност към определена група лекарства. Лекарствата се прилагат, като правило, чрез лумбална пункция, тъй като именно този подход позволява да се постигне максимален ефект от лекарствата. За монокурс на химиотерапия най-често се предписва метотрексат. Ако е необходимо комбинирано използване на средства, предпочитание се дава на цитарабин, темозоломид или етопозид. Изборът на лекарства остава само при лекуващия лекар. Курсът на химиотерапия има много странични ефекти и често може да провокира влошаване на благосъстоянието на пациента, но рискът от свръхрастеж на неоплазмата оправдава целесъобразността на използването му. Страничните ефекти възникват в резултат на увреждане на здрави клетки, тъй като, за съжаление, химиотерапията не може да убие само раковите клетки, без да засегне здравите. Честотата и интензивността на определени прояви зависи от дозата и вида на избраното лекарство. Честите нежелани реакции на химиотерапията включват:
обикновено са лечими с курс на химиотерапия. Може да се предпише курс на моно- или полихимиотерапия. В зависимост от вида на лимфома и неговата чувствителност към определена група лекарства. Лекарствата се прилагат, като правило, чрез лумбална пункция, тъй като именно този подход позволява да се постигне максимален ефект от лекарствата. За монокурс на химиотерапия най-често се предписва метотрексат. Ако е необходимо комбинирано използване на средства, предпочитание се дава на цитарабин, темозоломид или етопозид. Изборът на лекарства остава само при лекуващия лекар. Курсът на химиотерапия има много странични ефекти и често може да провокира влошаване на благосъстоянието на пациента, но рискът от свръхрастеж на неоплазмата оправдава целесъобразността на използването му. Страничните ефекти възникват в резултат на увреждане на здрави клетки, тъй като, за съжаление, химиотерапията не може да убие само раковите клетки, без да засегне здравите. Честотата и интензивността на определени прояви зависи от дозата и вида на избраното лекарство. Честите нежелани реакции на химиотерапията включват:
- гадене и повръщане;
- обща слабост, неразположение, причинено от анемия;
- косопад;
- потискане на имунните функции на организма, в резултат на по-голяма чувствителност към инфекции;
- сухота в устата и образуване на язви и рани в неговата кухина;
- нарушение в стомашно-чревния тракт.
Лъчетерапия
излагане на радиация като независим методсе използва рядко, по-често се комбинира с курс на химиотерапия или операция. В късен стадий на заболяването лъчетерапията се използва като палиативен метод за облекчаване на състоянието на пациента чрез намаляване на тумора и притискане на здравите му тъкани. Страничните ефекти от лъчетерапията могат да бъдат от различно естество в зависимост от мястото на облъчване. Що се отнася до въздействието на радиацията върху мозъка, негативните прояви могат да се появят след няколко години. Те се изразяват, като правило, под формата на неврологични разстройства. С комплексния ефект от курса на химиотерапия и излагане на радиация, негативните последици от първото могат да се влошат.
 Лимфомът на Бъркит е практически нелечим с операция. Причината за това е специфичното местоположение и тип на растеж на образуванието. Фоликуларният лимфом и много от другите му видове улавят различни мозъчни клетки, например местоположението на основния тумор може да бъде в малкия мозък, а микроскопичните атипични клетки могат да бъдат разпръснати из целия орган. В тази връзка е почти невъзможно да се извърши радикален тип операция. Те прибягват до хирургическа интервенция, за да отстранят максималната част от образуването, за да намалят растежа на тумора и да вземат материала за биопсия, след което използват курс на химиотерапия или радиация, за да унищожат останалите атипични клетки.
Лимфомът на Бъркит е практически нелечим с операция. Причината за това е специфичното местоположение и тип на растеж на образуванието. Фоликуларният лимфом и много от другите му видове улавят различни мозъчни клетки, например местоположението на основния тумор може да бъде в малкия мозък, а микроскопичните атипични клетки могат да бъдат разпръснати из целия орган. В тази връзка е почти невъзможно да се извърши радикален тип операция. Те прибягват до хирургическа интервенция, за да отстранят максималната част от образуването, за да намалят растежа на тумора и да вземат материала за биопсия, след което използват курс на химиотерапия или радиация, за да унищожат останалите атипични клетки.
Ако ракът на мозъка е в ранен стадий и размерът на неоплазмата не е впечатляващ, а мястото на локализацията му позволява операция, можем да говорим за успех на метода и положителен резултат след операцията. Но във всеки случай, за да се гарантира, че всички ракови клетки са унищожени, въпреки началния стадий на заболяването, на пациента се препоръчва да премине курс на химиотерапия, за да консолидира резултата.
Прогнозата зависи от стадия, вида на лимфома и местоположението му. Младите пациенти понасят рак малко по-лесно и имат по-добра преживяемост от по-възрастните пациенти. Без спешно започнато лечение ракът с локализация в медиастинума или мозъка много бързо засяга работата им и води до смърт след няколко месеца. С правилно подбрана навременна терапия 40% от пациентите могат да преодолеят петгодишния етап.
Четенето укрепва невронните връзки:
лекар